
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




19世紀,病理學之父魯道夫·魏爾肖 (Rudolf L.K. Virchow,1821~1902)提出疾病的本質在於特定細胞的損傷。在臨床治療中,非靶向組織細胞受損是疾病並發症和不良反應發生的主要誘因,如藥物接觸部位、富集區域、代謝部位(如肝)、排泄部位(如腎)等非靶向組織的細胞損傷將容易引發更多的並發症和不良反應,影響臨床治療效果和患者生存質量。
隨著人口素質和經濟水平的提高,預防和修複細胞受損將是精準治療需考慮的重要因素,參與細胞損傷修複的藥物將具有極強的剛性需求。同時,伴隨著基因組學、蛋白質組學和檢測技術的快速發展,一些內源性物質對於細胞損傷的修複作用被發掘,其中輔酶I(NAD)是近年來醫學界最關注的研究對象。
輔酶Ⅰ匱乏,細胞損傷重要誘因
輔酶Ⅰ(NAD),化學名煙酰胺腺嘌呤二核甘酸或二磷酸煙苷,在哺乳動物體內存在氧化型(NAD+)和還原型(NADH)兩種狀態,作為生物催化反應必不可少的輔酶,參與上千種生理反應,如細胞三羧酸循環(TCA)、脂肪β氧化、酒精代謝等過程,尤其在糖、脂肪、氨基酸等營養物質的代謝利用過程中擔任十分關鍵的角色。
眾所周知,能量代謝對全身細胞的正常生理功能有著極其重要的意義,特別是心肌、神經元等耗能大的細胞。臨床上心功能不全症狀大多與心肌能量不足密切相關,首都醫科大學附屬安貞醫院副院長周玉傑表示,心力衰竭時主要的病理變化是心肌重構和心肌纖維化,心肌重構使單位重量心肌的毛細血管數量減少,氧彌散距離增大,心肌因而相對缺氧;此外,心力衰竭時心肌中ATP酶的活性可降低20%~40%,使心肌能量的利用發生障礙,心肌收縮力因而減弱;心力衰竭時還可能有線粒體結構異常,氧化磷酸化過程受損,線粒體中電子轉運鏈複合物活性和ATP的產生均降低或減少。“眾多輔酶類藥物作為電子傳遞的載體,在心肌線粒體氧化磷酸化過程中發揮著重要的作用,參與ATP的合成和代謝。心力衰竭時由於存在明顯的心肌能量代謝受損,因此,應根據患者不同情況,調控其心肌能量代謝。能量代謝各個環節的藥物對於改善心力衰竭症狀,均有一定效果。”
氧化型輔酶Ⅰ(NAD+,下文統稱輔酶I)在線粒體內經過TCA循環中接受電子傳遞還原成還原型輔酶Ⅰ(NADH),通過電子傳遞能夠抑製自由基生成,增加穀胱甘肽含量,抑製細胞色素C從線粒體釋放,維持線粒體的正常功能;作為電子傳遞鏈最重要的氫供體,1mol輔酶Ⅰ參與3mol ATP的生成,是細胞生命活動能量合成中最關鍵的輔酶。值得一提的是,輔酶Ⅰ(NAD)的抗氧化能力是輔酶類物質中最強的,強於輔酶Q10。另外,輔酶Ⅰ在體內的代謝物如輔酶Ⅱ、煙酰胺(NAM)、ADP核糖等物質在人體細胞能量代謝、氧化壓力調節和信號通路傳遞方麵意義重大。
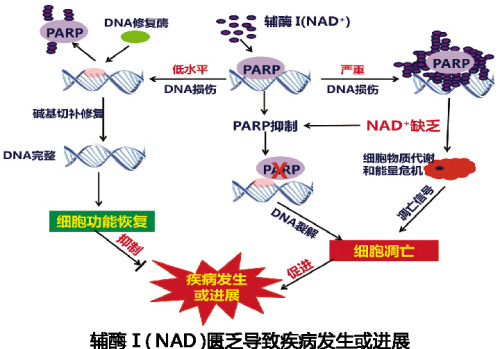
輔酶Ⅰ匱乏是疾病發生和進展的重要因素之一。急性創傷、炎症、缺氧、輻射、化學毒物等因素會造成體內自由基大量增加,導致細胞DNA嚴重受損。為應對這種損傷,細胞內DNA修複酶PARP自動大量激活,它需持續消Ⅰ來進行修複,從而造成細胞內輔酶Ⅰ匱乏。直接後果是線粒體功能受到抑製,ATP生產減少,細胞能量不足,凋亡信號被激活並釋放,最終細胞凋亡。同時其它NAD+依賴性酶(Sirtuins、CD38等)受到影響,信號通路受阻,細胞活力減弱,細胞正常生理功能被抑製,最終加速疾病發生或進展。
輔酶Ⅰ,理想的細胞損傷修複劑
隨著國內外研究的深入,輔酶Ⅰ更多生理功能機製被揭示,其中最重要的發現是,它是NAD+依賴型ADP核糖基轉移酶的唯一能利用的物質,這類酶將輔酶I作為底物分解成ADP核糖和煙酰胺(Nam),在不同細胞中發揮不同生理功能。這類酶在體內主要有三種: 1.ADP核糖基轉移酶或聚核糖基聚合酶(PARP),參與DNA修複、基因表達、細胞周期進展、細胞存活、染色體重建和基因穩定性等;
2.環ADP核糖合成酶(cADPR synthases)環核糖聚合酶(cADP合酶),它是由一對細胞外酶組成,這對外酶就是熟悉的淋巴細胞抗原CD38和CD157,它們以輔酶Ⅰ為底物生成環ADP核糖——重要的鈣信號(calcium signaling)信使,在鈣穩態維持方麵和免疫應答方麵具有重要生理意義;
3.Ⅲ蛋白型賴氨酸去乙酰化酶Sirtuins,為一類組蛋白去乙酰化酶,在哺乳動物內有7種不同的亞型(SIRT1-SIRT7),調節多種細胞功能,在細胞抗逆性、能量代謝、細胞凋亡和衰老過程中具有重要作用。Sirtuins對代謝平衡的調節同樣可以直接影響與代謝相關的各種疾病,如SIRT1在輔酶I的參與下調節組蛋白的乙酰化狀態,對增強心髒耐受氧化應激反應、調節心肌能量代謝及抗衰老等起著重要作用。
在國內對還原型輔酶I(NADH)有著深厚學術造詣和研究成果的南方醫科大學珠江醫院腫瘤中心主任張積仁指出,NAD+和NADH的生理效應、生物代謝、藥理作用等方麵都存在差異性,迄今為止國外對於NADH的應用和研究已經十分成熟,而針對NAD的研究國內外還存在較大空白。“NADH藥物在中國還沒有上市,國內對NADH產品的相關研究仍處於比較局限的細分領域。不過,NAD產品在國內已經有企業生產並上市,未來輔酶領域的研究方向將進一步趨向於轉化醫學以及製備技術(提取、分離、純化)的研究。”相關文獻資料顯示,還原型輔酶I在國外已率先被應用於治療多種疾病,如改善帕金森氏綜合征症狀、減輕抑鬱症狀、改善慢性疲勞和免疫功能低下綜合征等。大量臨床應用未出現任何嚴重不良反應,被FDA批準作為營養補充劑進行使用。
值得注意的是,國內外對氧化型輔酶Ⅰ的研究也開始不斷重視,並逐漸湧現出大量成果。2012年,澳大利亞研究人員發現在年齡增長過程中,累積的DNA氧化損傷會引起DNA修複酶PARP的過量表達,加劇組織內輔酶Ⅰ的消耗。組織細胞內的輔酶Ⅰ消耗會限製能量合成、DNA修複和基因信號傳導等過程,在人體衰老過程中有著重要作用。大量研究發現,神經纖維、心肌細胞、腎髒細胞損傷過程中伴隨著輔酶I含量顯著降低。通過外源性補充可以恢複細胞內輔酶I的含量,進而降低因功能退化和缺血引起的神經纖維凋亡或氧化壓力介導的心肌細胞或腎髒細胞凋亡。除此之外,在急性炎症情況下,輔酶Ⅰ會被大量釋放到炎症組織,隨著細胞外的輔酶Ⅰ濃度升高,免疫細胞會向炎症病灶聚集,提高免疫應答能力。細胞水平研究發現,輔酶Ⅰ可通過激活和促進先天免疫細胞成熟、產生抗炎因子和抑製調節性T細胞等作用,保護免疫細胞(如白細胞),調節機體免疫力。
輔酶I開啟細胞損傷修複新篇章
基於大量基礎醫學研究證據,體外補充輔酶Ⅰ可有效提高細胞內輔酶Ⅰ含量,增強組織細胞代謝功能和抗氧化能力,有效抑製細胞損傷或凋亡,恢複細胞正常功能。作為細胞修複過程中的“引擎”和“燃料”,輔酶Ⅰ一方麵被NAD+依賴性ADP核糖基轉移酶用來啟動修複細胞損傷的程序,促進細胞DNA修複、抑製細胞凋亡信號產生,另外一方麵被用於促進營養物質代謝和ATP合成,為受損細胞提供充足的物質和能量,促進細胞恢複。同時,作為內源性物質,輔酶Ⅰ生物利用度高,不增加肝腎負擔,是一種理想的細胞損傷修複劑。
通過查詢CFDA藥品數據庫,發現以輔酶Ⅰ為單獨成分的製劑隻有一種——注射用輔酶Ⅰ。作為細胞代謝過程的必需物質和NAD+依賴性ADP核糖基轉移酶的唯一能利於的物質,它具有促營養和能量代謝、抗細胞氧化損傷和調節免疫的三重功能,在臨床上可以用於預防和治療多種疾病,如減輕缺血再灌注損傷、抑製細胞凋亡、抵抗和修複輻射或化學藥物毒性、增強機體免疫等作用;同時,作為內源性物質,注射用輔酶I生物利用度高,不增加肝腎負擔,臨床應用前景廣闊。
 相關新聞
相關新聞