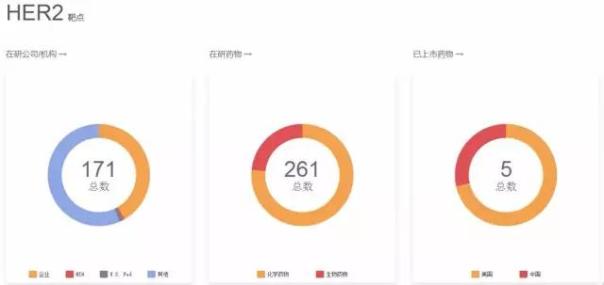
HER2是重要的乳腺癌預後判斷因子,針對該靶點開發的靶向藥物種類多樣。火石創造(微信:firestone-link)的靶點追蹤係統的數據顯示,目前已在美國上市的HER2靶向藥物有5種,其中兩種在中國上市。除此以外,許多關於HER2基因的多項新型藥物也正在臨床試驗中。
HER2受體及其靶向藥物
原癌基因人類表皮生長因子受體2(human epidermal growth factor receptor-2,HER2),即c-erbB-2基因,因無可溶性的配體而被稱為“孤兒受體”。該受體的聚合作用會導致酪氨酸殘基磷酸化,並啟動多種信號通路導致細胞增殖和癌症發生。
據臨床統計,15%~30%的乳腺癌和10%~30%的胃/食管癌會發生HER2基因擴增或過表達。此外,在卵巢癌、肺癌、膀胱癌、頭頸癌中也發現HER2基因的過表達。近年來,針對HER2靶點設計的藥物一直是研究的熱門,火石創造(微信:firestone-link)的靶點追蹤係統顯示,全球共有171家公司/機構正在研發HER2靶向藥物。
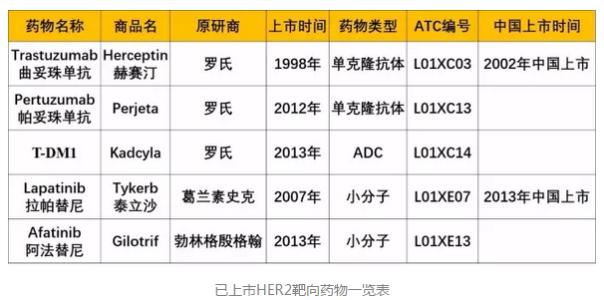
目前,已經有5種HER2靶向藥物通過了FDA審批,其中兩種獲CFDA批準在國內上市。
抗HER2的三種大分子藥物
在HER2靶點藥物的開發上,羅氏成績顯著。目前已上市的5種藥物中,3種均由羅氏原研,分別是曲妥珠單抗、帕妥珠單抗以及Kadcyla。
專利到期赫賽汀年銷售額下滑
1998年,赫賽汀(曲妥珠單抗)獲FDA批準上市。作為最早上市的HER2靶向藥物,赫賽汀主要適用於乳腺癌、胃癌、胃食管交界腺癌。赫賽汀於2000年在歐洲上市,2001年在日本上市,中國CFDA也在2002年批準了赫賽汀的上市銷售。
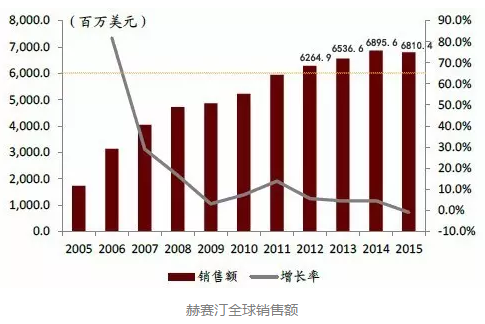
作為羅氏的原研產品,2012年,赫賽汀全球銷售額突破60億美元,之後一直保持穩定。由於2015年赫賽汀在美國的專利到期,大量仿製藥開始上市,導致價格下滑,市場規模也隨之出現萎縮。
乳腺癌是我國女性發病率最高的癌症,每年有近20萬女性被診斷出乳腺癌。赫賽汀作為治療HER2陽性乳腺癌的一線用藥,在我國有很大的市場剛性需求。2002年CFDA批準赫賽汀在中國上市以來,該產品在國內重點醫院的年銷售額一直保持著增長趨勢,至2015年達到了6.6億人民幣。
但是赫賽汀治療費用偏高,國內滲透率仍比較低。而考慮到赫賽汀已過了專利保護期,未來大批仿製藥的出現以及更多的省市將其納入醫保目錄,將有可能使赫賽汀在國內的滲透率快速提升。
被稱為“HER二聚化抑製劑”的帕妥珠單抗
Perjeta(帕妥珠單抗)是針對HER2的單克隆抗體藥物。最初由Genentech公司研發,2009年羅氏收購Genentech並掌握Perjeta。2012年Perjeta被FDA批準上市,2013年該藥品在歐洲和日本上市,全球銷售額快速增長,2015年突破15億美元,現已成為乳腺癌的二線治療藥物,但我國CFDA目前還未批準Perjeta在國內市場銷售。
帕妥珠單抗可阻斷HER2受體的二聚化,從而阻滯該受體被激活,但它和配體的結合位點與曲妥珠單抗不同,被批準與曲妥珠單抗和多西他賽等聯合用於未經激素治療或化療等既往治療的HER2陽性轉移性乳腺癌患者。
新型抗HER2的ADC藥物
大多數HER2陽性轉移性乳腺癌患者最終會產生耐藥性。Kadcyla(ado-trastuzumab emtansine,簡稱T-DM1)同為羅氏研發,是由曲妥珠單抗和細胞毒性組成的ADC藥物,它可以靶向作用於HER2過表達細胞來克服耐藥機製。
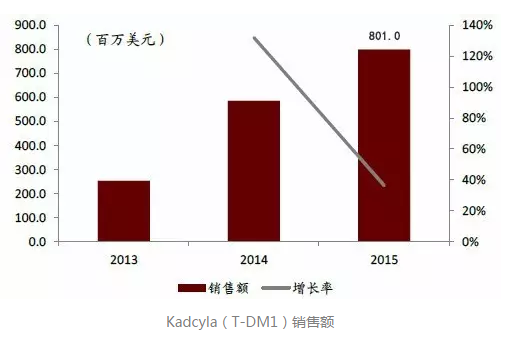
Kadcyla於2013年獲FDA批準上市,作為單藥用於經曲妥珠單抗和紫杉醇藥物分別或聯合既往治療的HER2陽性轉移性乳腺癌患者。同年,該藥在日本和歐洲相繼獲批上市,同Perjeta一樣,現已成為乳腺癌二線治療藥物,2015年全球銷售額突破8億美元。
FDA批準Kadcyla時有一項黑框警告,提醒患者和醫生:該藥可引起肝髒毒性、心髒毒性和死亡,在使用前要進行妊娠試驗。目前CFDA還未批準該藥在國內上市。
抗HER2的兩種小分子藥物
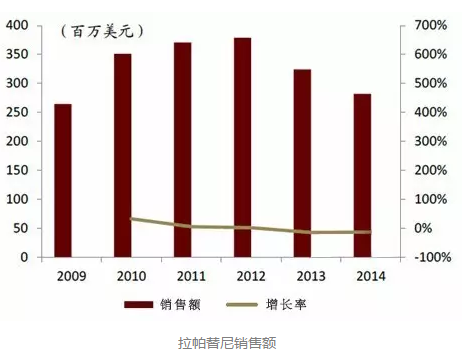
銷量相對較小的泰立沙
泰立沙(拉帕替尼)是另一種在中國上市的HER2靶向藥物,於2007年獲FDA批準上市,2008年在歐洲上市,2013年被CFDA批準在中國上市。
泰立沙是由葛蘭素史克(GSK)原研的一種口服小分子表皮生長因子絡氨酸激酶抑製劑,被批準可與卡培他濱聯合用於經蒽環類藥物、紫杉醇及曲妥珠單抗既往治療的HER2過表達的晚期或轉移性乳腺癌患者。作為小眾藥,小分子口服製劑泰立沙銷量相對較小。
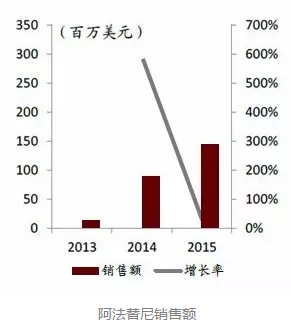
通過FDA孤兒藥認證的阿法替尼
另一種小分子HER2靶向藥物是Gilotrif(阿法替尼),它於2013年獲FDA批準上市,由勃林格殷格翰原研並銷售。該藥適用於晚期非小細胞肺癌(NSCLC)的一線治療及HER2陽性的晚期乳腺癌患者。
此外,阿法替尼還通過了FDA的孤兒藥認定。歐盟藥物管理機構於2013年核準“阿法替尼”用於醫治因表皮生長因子受體(EGFR)突變的非小細胞肺癌患者。中國台灣地區行政院衛生署食品藥物管理局(TFDA)也於2013年核準阿法替尼藥物上市。
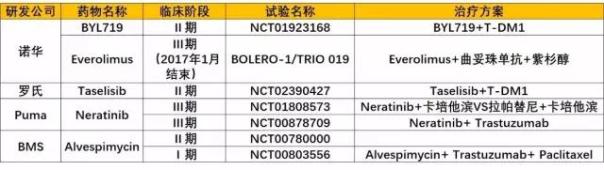
基於火石創造已有的數據持續更新的靶點追蹤係統,我們可以了解到更多關於HER2陽性轉移性乳腺癌的多項新型藥物正在臨床試驗中,下表羅列了部分已完結和在研的新型藥物,更多信息可以登錄火石官網查看。















 相關新聞
相關新聞