抗體類藥物在腫瘤領域可謂大放異彩。2015年《Nature》發表的“Nature Reviews Cancer”回顧了全球抗腫瘤藥物的發展史,文章特別強調抗體類藥物在腫瘤治療中的臨床地位。
事實上,抗體類藥物已不僅僅用於抗腫瘤治療,還用於多種自身免疫疾病、心腦血管疾病、眼科疾病等治療領域。
抗體類藥物開發已經進入成熟階段。早期主要是解決免疫原性問題,上世紀80年代以前的單抗主要是鼠源抗體,包括免疫原性反應在內的安全性問題使其難以得到臨床認同。近年來,全人源抗體技術已經不是難題,最新的抗體藥物已經實現全人源化,可完全規避鼠源成分帶來的各種安全性風險。
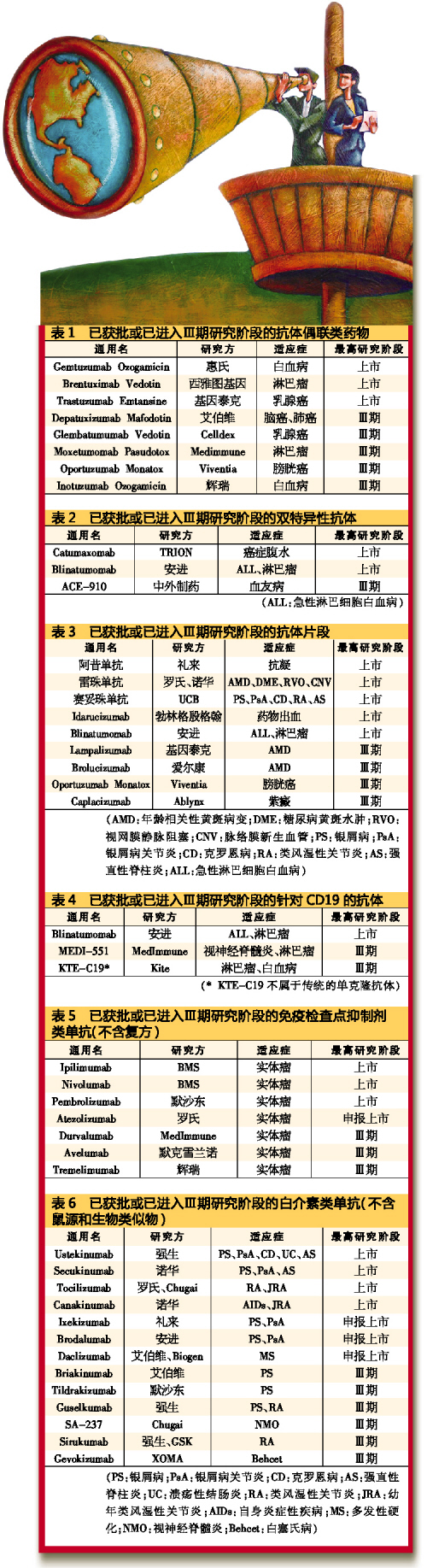
根據湯森路透的數據,目前已獲批或至少進入Ⅲ期臨床研究的抗體類藥物共有243個,其中114種品種已經獲批。243個抗體類藥物中,有163個屬於創新藥,另有80個是生物類似物。
需要指出的是,抗體類藥物實質並非僅指單克隆抗體,還包括單克隆抗體片段以及受體-抗體FC融合蛋白。文中的抗體類藥物是單抗藥物、抗體片段藥物和融合蛋白藥物的總稱。
那麽,哪些新技術和新靶點將主宰未來的抗體類藥物研發方向?
【新技術】
三大開發熱點方向
如何通過抗體的工程化,設計更有針對性、更能解決臨床問題的新型抗體,是抗體類發展的又一個方向。這個方向包括抗體片段、雙特異性抗體和抗體偶聯物等研發熱點,以雷珠單抗、Blinatumomab和Kadcyla為代表的新型單抗陸續獲批。
抗體偶聯物:新技術平台扭轉局勢
抗體偶聯藥物(antibody-drug conjugate,ADC)將抗體和細胞毒性藥物通過偶聯子連接起來,這樣就能在發揮抗體靶向作用的同時,加強細胞毒藥物攻擊癌細胞的作用。
早在16年前,第一個抗體偶聯物惠氏的Gemtuzumab Ozogamicin就已獲批,然而該藥並不理想,不佳的療效和較為嚴重的副反應使得該藥淡出市場,這也導致ADC藥物的研發一度受到影響。
不過,新的技術平台改進了偶聯技術。西雅圖基因、基因泰克研發的新一代ADC品種Brentuximab Vedotin(Adcetris)和Trastuzumab Emtansine(Kadcyla)分別於2011和2012年獲批,改變了大眾對ADC藥物的擔憂。2014年,這兩個品種年銷售額分別為3.6億和5.9億美元。其中,Kadcyla利用經典的曲妥珠單抗作為抗體,聯合微管蛋白抑製劑DM1能達到曲妥珠單抗聯合紫杉醇的協同治療效應,業內看好其年銷售額將超過29億美元。
除了以上3個已經上市的品種,目前已經進入Ⅲ期臨床的在研化療類ADC藥物還包括:艾伯維的Depatuxizumab Mafodotin、Celldex的Glembatumumab Vedotin、Medimmune的Moxetumomab Pasudotox、Viventia的Oportuzumab Monatox和輝瑞的Inotuzumab Ozogamicin。其中,Depatuxizumab Mafodotin是針對EGF的單抗和細胞毒類微管蛋白抑製劑結合的偶聯劑,理論上適用於NSCLC等多種實體瘤。
雙特異性抗體:成熟技術帶來更多機會
傳統的單克隆抗體通過抗體FAB結合2個抗原,但這兩個FAB段的結合點隻能結合1種抗原。讓單克隆抗體結合多個抗原是抗體藥物研究的熱點方向,其中相對成熟的是雙特異性抗體(BsAb)。BsAb含有兩種特異性抗原結合位點,能分別與靶細胞上的抗原和抗癌(病)細胞(分子)的抗原結合,搭建抗癌橋梁,激發具有導向性的免疫反應。
早期的BsAb研究技術較為局限,產生的BsAb並不理想。不過,近年來安進、基因泰克等都加快了BsAb的研發,包括knobs-into-holes、BiTEs等新技術不斷成熟,使得BsAb藥物有了更多機會。
目前已有2個BsAb藥物獲批。Catumaxomab是第一個獲批的BsAb,為抗上皮細胞粘附分子和抗CD3的雙特異性抗體。Catumaxomab屬於特殊的Triomab(三功能抗體),它可以同時靶向腫瘤,通過結合CD3招募T細胞,並通過結合FCγ受體激活單核細胞、巨噬細胞、樹突細胞和NK細胞。不過Catumaxomab是鼠源抗體,且僅獲得癌症導致的腹水一個適應症,故市場前景並不理想。真正得到臨床認可的雙特異性抗體是安進的基於BiTE技術開發的Blinatumomab,該藥同時靶向癌細胞的CD19抗原和T細胞的CD3抗原,對難治或複發的急性淋巴細胞白血病完全緩解率高達43%,對淋巴瘤也有不錯的療效。
在研藥物中,禮來的Emibetuzumab、羅氏的抗腫瘤BsAb等也都進入了Ⅱ期臨床。
需要指出的是,雙特異性抗體並非抗癌藥物獨有,該技術生產的單抗也有望用於其他疾病,如自身免疫疾病、眼科疾病等。其中,該技術用於治療血友病的ACE-910已進入Ⅲ期臨床研究階段。
抗體片段:小型化更易穿透腫瘤
單克隆抗體還有一個重要發展方向是小型化。一般認為,抗體片段比完整的抗體更為優越,更有可能透過血腦屏障,並能降低抗體與Fc受體的非特異性結合。
目前抗體片段的發展有3個方向——Fab片段、單鏈抗體(ScFv)和納米抗體(nanobody)。其中,Fab片段最為成熟,單鏈抗體已經成為開發雙特異性抗體的一個重要方式,而納米抗體還沒有成功獲批的品種。
目前已獲批或進入Ⅲ期臨床研究階段的抗體片段共有9個,其中Fab片段類藥物最多,共有5個,包括在眼科領域大紅大紫的雷珠單抗。雷珠單抗是人源化重組抗VEGF單克隆抗體片段Fab部分,可用於年齡相關性黃斑病變等眼科疾病,2014年全球銷售總額超過43億美元。UCB的賽妥珠單抗是聚乙二醇人源化Fab片段的抗INF-α單克隆抗體,該藥同時具有Fab片段的優點和長效製劑的優勢,被認為有取代英夫利西單抗並與阿達木單抗競爭的潛質,2014年該藥銷售額為11億美元。阿昔單抗(abciximab)是FDA批準的首個抗體片段,該藥是抗血小板凝聚單克隆抗體Fab,是抗凝作用最強的藥物之一,但免疫原性反應、不可逆性和非特異性不足的特性影響了該藥的使用。
相比於Fab,ScFv更小,其分子量隻有前者的一半,由於穩定性不佳,其一般用於製作雙特異性抗體和抗體偶聯物,其中雙特異性抗體Blinatumomab就屬於ScFv。
Nanobody是Ablynx公司專利納米抗體技術,該技術生產的抗體片段隻包括一個重鏈可變區,分子量隻有單抗的十分之一,因此更容易穿過腫瘤。目前以該技術為基礎開發的Caplacizumab已進入Ⅲ期臨床,該藥可用於血小板減少性紫癜。
【新靶點】
有重大突破的三大靶點
傳統用於腫瘤和自身免疫疾病治療的抗體類藥物治療靶點主要局限在CD20、ErbB2、VEGF、EGF上,由於現有單抗依然對部分腫瘤和自身免疫疾病治療不甚理想,故臨床希望開發一些新靶點的單抗,其中最為熱門的無疑是PD-1類。
CD19:與雙特異性抗體、CAR-T共振
CD19是B細胞表麵的跨膜蛋白,它與B細胞活化、信號傳導及生長調節密切相關,是一係列血液係統腫瘤治療的新靶點。
針對CD19的單克隆抗體有多個在研藥物,其中MedImmune的MEDI-551已進入Ⅲ期臨床研究,正在開展針對視神經脊髓炎、B細胞淋巴瘤和多發性硬化的相關研究。
CD19單抗在抗體偶聯物和雙特異性抗體也擁有機會,目前有多個在研的CD19抗體偶聯物,其中西雅圖生物的Denintuzumab Mafodotin已經進入Ⅱ期臨床。
雙特異性抗體目前最成功的靶點是抗CD19+CD3,安進的Blinatumomab同時靶向癌細胞的CD19抗原和T細胞的CD3抗原,該藥已經於不久前獲批,市場反響強烈。
關於CD19單抗,還有一個不得不說的類型,就是大名鼎鼎的CAR-T。雖然CAR-T療法屬於細胞療法,不屬於傳統的抗體藥物,但CAR-T藥物的核心就是將單克隆抗體嵌入治療細胞中,誘導T細胞攻擊癌細胞,目前絕大部分CAR-T藥物都選擇CD19為靶點,其中KTE-C19已經進入Ⅲ期臨床並獲得了FDA的突破性認定。
免疫檢查點:腫瘤免疫療法的一個高潮
免疫檢查點抑製劑和CAR-T是抗腫瘤藥物治療的兩大重要突破,也將腫瘤免疫治療推到了一個高潮。2014年《Forbes》破例將兩個腫瘤免疫藥物分別是Opdivo(Nivolumab)和Keytruda(Pembrolizumab)列為該年度最重要的創新藥,二者均屬於免疫檢查點抑製劑。免疫檢查點被認為參與誘導癌細胞逃逸反應。
已發現的免疫檢查點主要包括CTLA4、PD-1、PD-L1、LAG3(淋巴細胞激活基因3)、B7-H3、B7-H4和TIM3(T細胞膜蛋白3)。其中前三類已相對成熟,有已獲批或Ⅲ期臨床藥物。
CTLA4抑製劑是最先研發的免疫檢查點抑製劑,2010年獲批的BMS的Ipilimumab是全球首個獲批的該類藥物,在化療難度大的黑色素瘤治療中該藥顯示了優越的療效,客觀緩解率從4個月延長到10個月,盡管安全性不佳,但該藥2014年全球銷售額依然超過13億美元。
在CTLA4的安全性問題受到關注時,PD-1抑製劑橫空出世。BMS的Opdivo(Nivolumab)和默沙東的Keytruda(Pembrolizumab)相繼獲批。兩個藥物治療黑色素瘤效果都非常不錯,Nivolumab治療晚期黑色素瘤的客觀緩解率達到32%,客觀緩解期超過6個月,Pembrolizumab則是取得了與優於Ipilimumab的療效。在更為關注的非小細胞肺癌治療上,兩個藥物的“答卷”同樣精彩,Nivolumab的客觀緩解率超過紫杉醇18個百分點,Pembrolizumab客觀緩解率則延長了2.7個月,此外兩個藥物的安全性表現也同樣令人滿意。業內預測Opdivo和Keytruda均有望年銷售額逾50億美元,位居全球暢銷藥前十位。
羅氏的Atezolizumab是進度最快的PD-L1抑製劑,該類藥物與PD-1有所相似,該藥正向FDA申請肺癌和膀胱癌適應症。
白介素類:研發最熱的TNF-a取代者
雖然腫瘤壞死因子類(TNF-a)單抗藥物在自身免疫疾病的治療中占據重要地位,但TNF-a藥物在治療中依然存在許多不足,一些新靶點的藥物在自身免疫疾病治療中可以補充或取代TNF-a藥物。其中,研究最為活躍的無疑是白介素類,主要針對的靶點包括IL-1、IL-2、IL-6、IL-12、IL-17、IL-23。
IL-12家族是自身免疫疾病研究的熱點,該家族包括IL-12和IL-23等,在體內主要表現出促炎作用,抑製IL-12和IL-23都能起到阻止自身免疫疾病炎症的作用。Ustekinumab是強生於2009年研發上市的全人源抗IL-12/IL-23單克隆抗體,該藥對於重度銀屑病等多種重度自身免疫疾病療效優於TNF-a抑製劑,2014年該藥的全球銷售額達19.4億美元。此外,抗IL-12/IL-23和單純抗IL-23的單抗Briakinumab、Tildrakizumab、Guselkumab也都進入了Ⅲ期臨床。
IL-17是T細胞誘導的炎症反應的早期啟動因子,可以通過促進釋放前炎性細胞因子來放大炎症反應,因此對IL-17的抑製能盡早阻斷炎症物質的釋放,消除自身免疫疾病炎症反應。Secukinumab是諾華最新獲批的全人源抗IL-17單克隆抗體,該藥完成了一項與Ustekinumab對比治療重度銀屑病的臨床研究,結果顯示Secukinumab療效顯著占優,湯森路透樂觀認為該藥2019年全球銷售額將達到16億美元。此外,處於申報上市的IL-17單抗還包括Ixekizumab和Brodalumab。
IL-6在體內有多種功能,其中該因子可以導致調節性T細胞失衡並分泌多種炎症物質。Tocilizumab是羅氏的人源化抗IL-6單抗,於2005年獲批,該藥主要針對TNF-a不應答的類風濕性關節炎,2014年該藥全球銷售額為13億美元。同類藥品還包括SA-237和Sirukumab。
IL-1β是一種炎症因子,存在於身體各個部位,廣泛參與組織破壞、水腫等炎症反應。該因子的失控會出現一係列表現各異的全身或局部自身炎症性疾病(autoinflammatory diseases,AIDs),如蛋白相關的周期性綜合征、白塞氏病、克羅恩病等。諾華於2009年獲批的Canakinumab就是IL-1β的單抗,適應症包括多種AIDs,在研的Gevokizumab也屬於同類藥物。
白介素類單抗值得期待的藥物還包括抗IL-2的多發性硬化用藥Daclizumab。
結語<<<
中國的抗體類藥物創新相較歐美還較為落後,目前在中國獲批的抗體類藥物創新藥僅有尼妥珠單抗和康柏西普等數個。
不過,中國的抗體類藥物創新水平正逐步趕上。一是國家新藥創製政策對生物藥創新日益重視,最新的“十三五”新藥創製計劃明確對抗體類藥物新技術和新靶點創新的支持,包括雙特異性抗體、抗體偶聯物、PD-1類藥物等都將給予重點支持。二是海外歸國高水平生物藥人才在國內陸續創建的生物藥創新企業為國內帶來了歐美最新的生物藥創新技術,也帶來了生物藥創新的新理念。三是風投等資本力量與生物藥創新的結合日益緊密。包括恒瑞的PD-1類藥物SHR1210、康方生物的免疫監測點抑製劑AK-107、信達生物的雙特異性抗體Anti-PD-1 Bispecific Antibodies等在研藥物的海外市場權益,都以數億美元的高昂價格轉讓給跨國企業,中國的創新抗體類藥物已逐步得到國外企業的認同。















 相關新聞
相關新聞