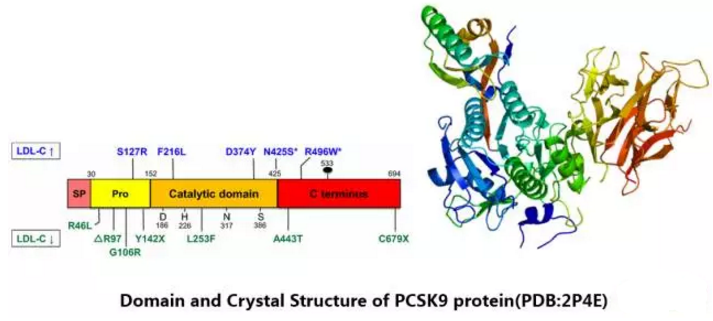
PCSK9簡介
在過去近十年裏,他汀類藥物是降脂治療的主力軍,該類藥物可以通過降低LDL-C進而減少心血管事件風險。近年來,PCSK9抑製劑成為脂質學藥物研發領域一顆耀眼的明星,從分子機製闡明到相應藥物上市僅10餘年時間間隔。大量研究顯示,該類藥物可以顯著降低LDL-C水平,多項臨床終點試驗也正在進行中。
2003年研究人員在一個法國家族中發現了PCSK9 (Proprotein convertase subtilisin / kexin type 9)的突變基因,這個基因也成為除LDLR和APOB之外的第三個與常染色體顯性家族性高膽固醇血症有關的基因。PCSK9 cDNA長度為3617bp,編碼692個氨基酸殘基組成的PCSK9蛋白。PCSK9基因的功能獲得性突變可導致常染色體顯性的家族性高膽固醇血症,使得LDL受體水平下降,從而導致LDL-C水平的升高。常染色體顯性的家族性高膽固醇血症與早發心血管疾病風險的增加密切相關。令人感興趣的是,PCSK9基因喪失突變功能可出現低水平的血漿LDL-C和apoB。多項大型流行病學研究發現,PCSK9基因變異後出現喪失突變功能與心血管事件的發生關係越來越密切。

Mechanism and role of PCK9 in low-density lipoprotein-cholesterol metabolism
正常人體中,LDL-R與LDL-C結合後形成複合物,並由網格細胞胞吞入肝細胞內,然後LDL-R與LDL-C解離重新回到肝細胞表麵。PCSK9能與LDL-C競爭性地結合肝細胞表麵的LDL-R,PCSK9的催化結構域能與LDL-R的表皮生長因子A (epidermal growth factor A,EGF-A)相互作用形成複合物,PCSK9/LDL-R複合物進入肝細胞到達溶酶體降解LDL-R,防止LDL-R再循環到肝細胞膜表麵。降低了肝細胞表麵的LDL-R,LDL-C不能被肝髒清除,血液中的LDL-C水平升高。在編碼PCSK9的基因發生功能獲得型突變後可增加對LDL-R的降解,從而使肝細胞表麵的LDL-R下調,血漿LDL-C水平升高。因此,抑製PCSK9的活性可以使血液中的LDL-C水平降低。
FDA批準的PCSK9抑製劑類藥物
通過PCSK9抑製來降低LDL-C已成為藥物研發熱點。目前PCSK9抑製劑中最為成熟的是單克隆抗體類藥物,其中Alirocumab以及Evolocumab已經被美國食品與藥品管理局(FDA)和歐洲藥品管理局(EMA)批準上市。

Alirocumab
由賽諾菲和再生元聯合研發,於2015年7月24日獲得美國FDA批準,2015年9月23日獲得歐洲EMA批準,2016年7月4日獲得日本PMDA批準上市,商品名定為Praluent。這是在美國獲批的首個前蛋白轉化酶枯草溶菌素9 (PCSK9)抑製劑類降膽固醇治療藥物。Alirocumab是一種全人源IgG1型單克隆抗體,作為PCSK9抑製劑,能結合PCSK9並抑製循環型PCSK9與低密度脂蛋白受體LDLR的結合,從而阻止PCSK9介導的低密度脂蛋白受體降解。該藥物用於治療成人雜合子型家族性高膽固醇血症和臨床動脈粥樣硬化心血管疾病(如需降低低密度膽固醇的心髒病或中風)。
Praluent是一種皮下注射用溶液,含75mg或150mg Alirocumab,推薦劑量為每次75mg或150mg,每兩周一次。Praluent最常見的副作用包括瘙癢、腫脹、疼痛、注射部位挫傷、鼻咽炎及流感。過敏性反應如過敏性血管炎(一種皮疹,通常表現為皮膚上的紫色斑點,與小血管的炎症相關)及需要住院的超敏反應在使用Praluent的患者中有報道。如果患者經曆嚴重過敏反應症狀,應該停止使用該藥並尋求醫療幫助。
在這一輪研發競賽中,安進的Repatha (Evolocumab)和賽諾菲/Regeneron的Praluent (Alirocumab)處於領先地位。有意思的是,在美國市場,安進Repatha原本處於領先地位,但賽諾菲在衝刺階段史無前例地花了6750萬美元買了一張加速審評券,使Praluent審查周期從正常的10個月縮短至6個月,實現快道超越安進。
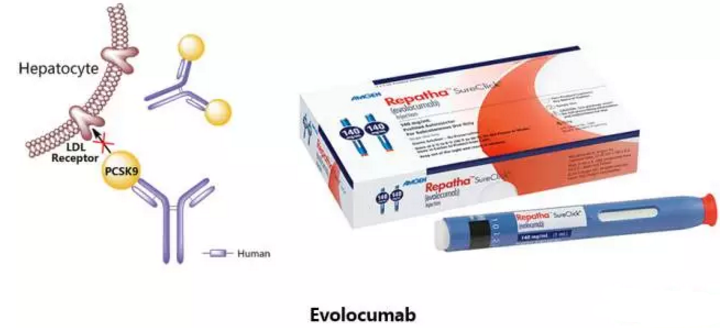
Evolocumab
由安進開發,於2015年7月17日獲得歐洲EMA批準,2015年8月27日獲得美國FDA批準上市,2016年1月22日獲得日本PMDA批準,商品名為Repatha。Evolocumab是一種全人源IgG2型單克隆抗體,作為PCSK9的抑製劑,能夠結合PCSK9並抑製循環型PCSK9與低密度脂蛋白受體LDLR的結合,從而阻止PCSK9介導的低密度脂蛋白受體降解。該藥物批準的適應症為高膽固醇血症和混合血脂異常。
Repatha是一種皮下注射液,每支預填充的注射器含140mg/ml的Evolocumab,推薦劑量為每次140mg,每兩周一次(成人原發性疾病)或每次420mg,每月一次(成人和12歲及以上兒童純合子型家族性膽固醇血症)。Repatha的最常見副作用包括鼻咽炎、上呼吸道感染、流感、背痛和給予注射處的反應,例如發紅、疼痛或淤傷。使用Repatha曾報道過敏反應如皮疹和蕁麻疹,如出現嚴重過敏反應,患者應停止使用該藥並尋求醫療幫助。
在研PCSK9抑製劑類藥物及其分類
作為最引人關注的藥物靶點之一,目前在研的PCSK9抑製劑類藥物較多,簡要按照不同研發策略總結如下:

單抗類藥物
單克隆抗體藥物是近年生物醫藥領域中的研發熱點,具有靶向性強、特異性高和毒副作用低等特點,代表了藥品治療領域的最新發展方向。以PCSK9為靶標的單克隆抗體可以與PCSK9發生特異性結合,從而阻斷PCSK9與LCLR的相互作用,減慢LCLR降解過程而發揮降低LDL-C水平的作用,也是最先取得突破的PCSK9抑製劑類藥物研究策略。
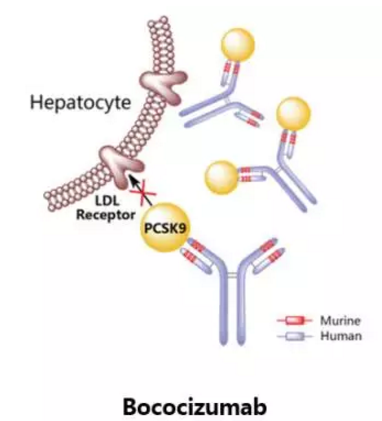
Bococizumab
輝瑞原研,是一種靶向於PCSK9的人源化IgGk型單克隆抗體,曾進行過治療高膽固醇血症的臨床三期研究,然而該項研究因結果未達預設終點而於2016年11月終止。輝瑞表示,通過對已獲得的Bococizumab臨床數據的全麵評估,以及深度權衡降脂新藥研發領域不斷變化的市場格局,該公司認為Bococizumab不大可能為患者、醫生及公司股東帶來價值,因此決定終止Bococizumab的全球開發項目。
RG7652
Genentech原研,後於2009年轉讓給Roche,用於治療包括帶有高冠心病風險的高膽固醇血症。在2013年開展的一項二期臨床試驗中,RG752表現出良好的藥物耐受性及顯著的劑量依賴性療效。盡管如此,由於至今未公開原因,Roche於2014年終止了該藥物相關臨床研究。
LY3015014
禮來原研。2016年初發表於《歐洲心髒雜誌》一項二期研究發現,LY3015014(一種處於研究階段的PCSK9抑製劑)聯合標準降脂治療能夠安全有效的改善高膽固醇血症患者的血脂異常。
LGT209
Norvatis原研,後轉讓給Cyon Pharmaceuticals Inc用於開展對服用他汀類藥物的高膽固醇血症患者的治療效果。該研究目前已被終止。
反義寡核苷酸類藥物
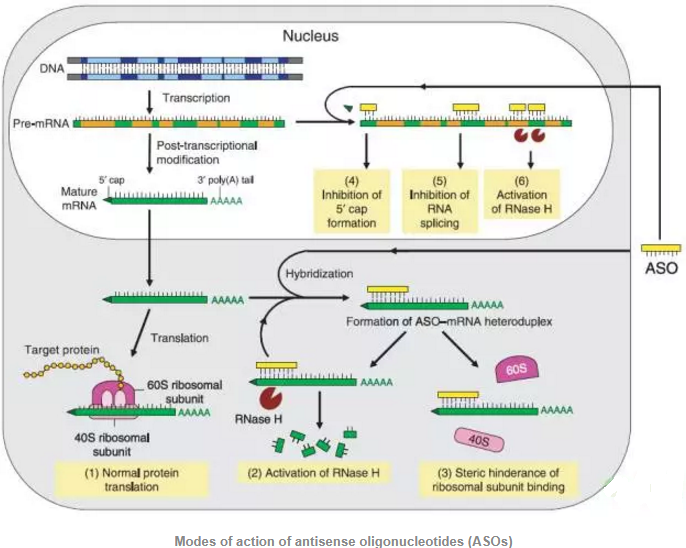
Modes of action of antisense oligonucleotides (ASOs)
反義寡核苷酸(antisense oligonucleotide,ASO)通常指進行了某些化學修飾的短鏈核酸(約15-25個核苷酸組成),它的堿基順序排列與特定的靶標RNA序列互補,進入細胞後可按照Watson-Crick堿基互補配對的原則與靶標序列形成雙鏈結構。反義寡核苷酸與靶標基因的RNA結合後可通過各種不同的機製影響靶標基因的表達。反義寡核苷酸類PCSK9抑製劑類藥物可以通過堿基互補原則結合於PCSK9靶基因mRNA上,從而封閉基因的表達,該類抑製劑在臨床前研究中表現出了良好的效果。
SPC5001
Santaris Pharma原研,後於2014年被Roche收購。該藥物在臨床前研究中表現良好,曾處於臨床一期研究,用於治療家族性高膽固醇血症,但目前該項研究已經終止。
BMS844421
百時美施貴寶與Ionis研發,曾進入一期臨床階段,現已終止,原因不明。
幹擾小RNA類藥物
幹擾小RNA (siRNA)可經由多種不同轉染技術導入細胞內,並對PCSK9基因產生具有專一性的基因敲除結果,在小鼠模型中可以顯著降低LDL-C水平。Alnylam公司最早於2008年開始探索采用RNA幹擾的方式阻止PCSK9蛋白的翻譯,並在2014年通過一期臨床研究證明其藥物平台是安全有效的。
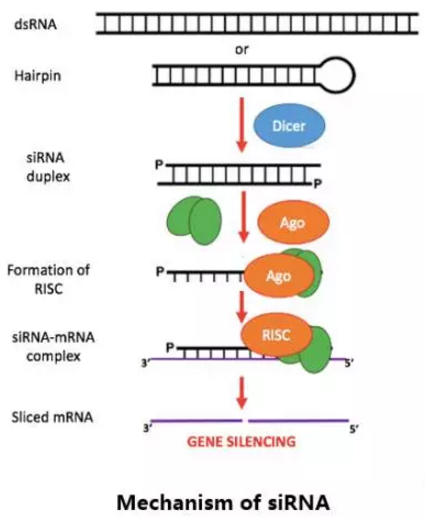
Inclisiran
Alnylam pharmaceuticals研發,采用Alnylam公司獨特的化學修飾工藝合成的靶向PCSK9 mRNA的RNAi療法。Alnylam公司將稱為GalNAc的一種糖分子與小幹擾RNA (Small Interfering RNA,siRNA)連接起來。這種經過修飾的siRNA不但更容易被細胞吸收,而且具備更高的穩定性,使得siRNA的療效更持久。
在被稱為ORION-1的臨床2期試驗中,497名高膽固醇患者在接受一次Inclisiran注射後的第60天,他們的LDL-C水平平均下降了51%,在接受注射後的第90天,LDL-C水平下降了45%。有189名高膽固醇患者在第1天和第90天分別接受了一次Inclisiran注射。這些患者在第120天LDL-C水平下降了57%,在第180天LDL-C水平下降了52%。這些指標與接受安慰劑治療的患者相比有非常顯著的統計學差異。這一結果意味著,高膽固醇患者一年可能隻需要少數幾次治療就可以控製住他們的膽固醇水平。2017年3月17日,基於良好的二期臨床表現,Alynylam Pharma宣布即將對Inclisiran開展三期臨床研究並有望在今年啟動,預計NDA申請將於2019年末左右提交。
ALN-PCS
Alnylam研發,靜脈注射,目前處於臨床一期研究階段。研究結果顯示,試驗組和對照組治療中不良反應時間發生率相同。ALN-PCS血藥濃度分布迅速,血藥濃度曲線大概以劑量成比例的方式增加。與對照組相比,ALN-PCS組別受試者血漿中PCSK9下降幅度平均為 70%,血漿中LDL水平下降幅度平均為40%。
ALN-PCSsc
Alnylam研發,皮下注射,目前處於臨床二期研究階段。初步試驗結果表明該藥物在降低膽固醇方麵可以媲美兩款最近獲得批準的強效注射劑藥物,並且其療效可以持續更長的時間,這意味著它可能隻需要每3-6個月給藥一次即可。與基於抗體的競爭產品PCSK9抑製劑不同,它們作用於血液,而這款新的皮下注射劑是一種新類型的治療藥物,它能夠阻止肝髒中與「壞」LDL膽固醇相關的蛋白的合成。
模擬抗體蛋白藥
模擬抗體蛋白藥是一種最新的生物治療方法,由連接不同類型分子的纖維結合蛋白組成,模擬抗體與靶點部位相結合的部分。該類別的PCSK9抑製劑類藥物可以通過阻斷PCSK9與LDLR的EGF-A結構域的結合從而發揮PCSK9的抑製作用。

DS‑9001
Pieris原研,後轉讓給Daiichi Sankyo繼續開發,目前處於一期臨床研究階段。Anticalin型蛋白為人工改造蛋白,可結合於蛋白或小分子等抗原。從結構上來說,Anticalin不同於抗體,屬於抗體模擬物。該蛋白可發揮同單克隆抗體同樣的功能,但分子量比一般抗體小8倍,通常由180個氨基酸殘基構成,分子量大約20kDa。Anticalin技術由Pieris Pharmaceuticals公司研發,並申請了相關專利。
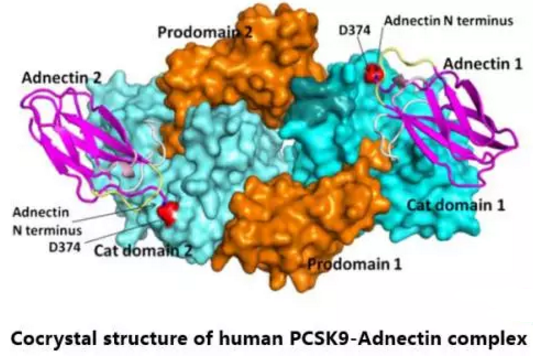
BMS‑962476
BMS原研,是PCSK9的Adnectin抑製劑,可作用另一種非抗體途徑。BMS-962476分子量約為11.3kDa,由103個氨基酸殘基組成。Adnectin是治療性蛋白,靶點結合親和力高,與抗體類似。第一個PCSK9的Adnectin抑製劑的研究顯示,它可迅速降低血漿中PCSK9和LDL-C的水平,且Adnectin介導的抑製有很好的耐受性。
1G08
Merck原研,為人類抗體-抗原結合片段,主要作用於PCSK9羧基末端結構域。與眾不同的是,1G08並不影響PCSK9與LDLR間的相互作用,而主要抑製PCSK9-LDL-R複合體的內吞過程而發揮活性。
小分子抑製劑類藥物
目前小分子PCSK9抑製劑類藥物的研發剛剛起步,尚處於生物活性研究階段。PCSK9這類靶點傳統上是不適合開發小分子的,它沒有像酪氨酸激酶那樣的天然口袋,結合界麵相對來說比較開放、平坦,小分子接觸麵積有限,產生的疏水作用力也不會太強(實際上小分子可能沒有被蛋白質包裹,直接裸露在水相環境中),即使結合上去了,被天然的大分子配體一碰可能就解離。
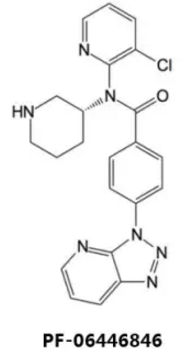
PF‑06446846
Pfizer公司建立了自己的表型篩選平台來篩選可阻斷PCSK9分泌進入血液的藥物,在250萬種化合物中篩選到了PF-06446846,也是唯一達到預設藥效和毒性閾值的Hit;隨後用了約5年時間闡明了該化合物作用的分子機製。功能研究表明,該化合物可結合於核糖體及剛翻譯出的PCSK9分子上,並阻塞核糖體退出通道,從而封閉PCSK9的產生。很多天然產物及抗生素也會抑製核糖體功能,但通常不具有特異性。而PF-06446846則與此不同,隻對包括PCSK9在內的約20種蛋白具有高度選擇性,且作用機製在從酵母到人類的真核生物中具有保守性。出於商業考慮等因素,目前Pfizer已終止了該藥物的研發,但隨著PCSK9研究的深入,希望之門並未完全關閉。
其他類別
MEDI4166
MedImmune原研,於2007年被阿斯利康收購,PCSK9抗體與GLP1多肽融合蛋白類藥物。目前處於臨床二期階段,用於治療成人2型糖尿病與心血管疾病。
AT04A
Affiris原研,疫苗類PCSK9抑製劑,目前處於一起臨床研發階段,適應症為動脈粥樣硬化。在2016年9月發表的一項研究報告中,AT04A能顯著降低小鼠模型的血液總膽固醇、甘油三酯及低密度脂蛋白濃度,降低血清中肝髒炎症標誌物含量,從而改善動脈粥樣硬化病情。
AT06A
Affiris原研,疫苗類PCSK9抑製劑,目前處於一起臨床研發階段,適應症為動脈粥樣硬化。Affiris公司一直致力於慢性病的疫苗類藥物開發,如帕金森及阿爾茨海默病等神經退行性疾病。
CRISPR-based approach
CRISPR技術有望實現“一勞永逸”的治療方式。來自Harvard大學的Kiran教授領導的團隊目前正致力於采用CRISPR-Cas9技術來降低PCSK9水平,小鼠實驗中可降低LDL-C達40%,且後續試驗表明,該策略在攜帶有人源化肝髒的嵌合體小鼠中同樣表現出色。製藥公司AstraZeneca同樣可開展了利用CRISPR技術抑製PCSK9的研究,相關結果有望近期發表。
前景與展望
以PCSK9為代表的新的降脂靶點受到越來越多的關注。科研界及醫藥工業界近十年的研發工作,使得PCSK9抑製劑的臨床研究取得了令人欣喜的進展,並在抗體藥物領域率先取得突破成為革命性降脂藥物。目前以單克隆抗體為代表的的生物製劑研發是新藥研發的熱點,在研的PCSK9抑製劑類抗體藥物也有多種。由於抗體藥物為注射劑型,而不是傳統的固體劑型,因而治療成本較高,且患者適應性也需要進一步的臨床觀察。但PCSK9抑製劑的研發將為降脂治療提供新的視角,尤其是對於他汀類藥物抵抗、難治性高膽固醇血症患者,PCSK9的臨床療效顯的更加明顯,長期安全性和耐受性良好,具有廣闊的臨床應用價值和前景。
























 相關新聞
相關新聞