
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




轉化醫學以藥物研發過程中生物標誌物為核心,以精準醫療提高藥物研發臨床應答率為目標,覆蓋從早期靶點確認——臨床前R&D ——臨床I、II、III期Development,到上市後的藥物檢測,通過不同階段的研究實現藥物研發的閉環。
hjc黄金城轉化醫學平台擁有經驗豐富的專業化技術團隊,從藥物靶點的作用機製和生物標誌物的臨床應用出發,以生物標誌物的發現和驗證為基礎,結合多種不同的技術平台和先進的儀器, 創建了多種生物分析方法,降低了藥物研發的成本和時間,為不同類型的藥物、不同類型的藥企和不同研發階段的項目提供多元高效的服務。
隨著基因組學、蛋白質組學和代謝組學等多組學分析技術不斷地發展,治療方式已經從傳統小分子擴展到多肽、蛋白、抗體、基因療法、細胞療法等多種新型技術。盡管有這些新技術,但仍有大量疾病的致病原因還無法徹底明白。轉化醫學將生物醫學觀察和研究轉化為改善健康的幹預措施的過程,加速了基礎研究、新藥開發的和臨床轉化的進程,成為精準靶向治療的加速器。轉化醫學研究利用各種研究手段,確定靶點與疾病發生發展的關係、驗證和探索藥物的作用機製、發現生物標誌物並開發伴隨診斷產品,以及為臨床研究開展篩選最合適的人群和適應症等,從而提高新藥研發效率和成功率。
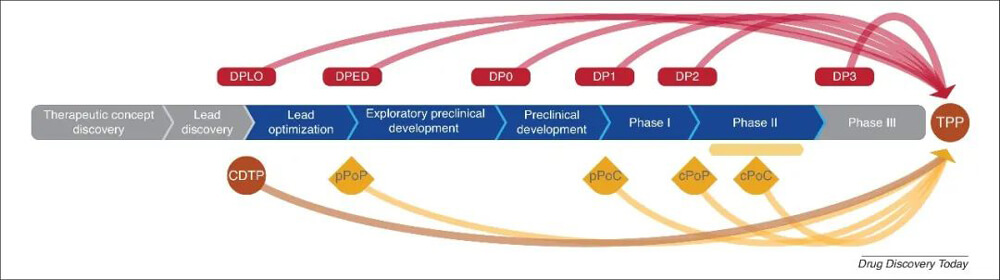
將轉化醫學裏程碑疊加到藥物開發階段[1]
生物標誌物(Biomarker)通常是指能被客觀測量和評價,反映生理或病理過程,以及對暴露或治療幹預措施產生生物學效應的指標。生物標誌物多來源於人體組織或體液,可涵蓋生理、生化、免疫、細胞和分子等水平的改變。
生物標誌物的檢測可廣泛地應用與病人的篩查、診斷、臨床研究、指導用藥、預後等領域。可提高基於基因組學、蛋白組學、細胞組學、病理組學等多組學的生物標誌物發現及驗證服務。為生物標誌物研究提供科學支持,多層麵助力新藥研發臨床試驗。生物標誌物作為最直接快速有效的診斷手段,其篩選與獲得可在疾病診斷、發展、治療、以及療效監測等多個方麵發揮重要的作用。生物標誌物有基於DNA的、有基於RNA的、還有基於蛋白質的,不同的分子和蛋白需要不同的技術平台。隨著高通量基因組學、蛋白質組學等的不斷進展,生物標誌物包括的種類也越來越多,例如SNP、外泌體、miRNA、lncRNA等都被列入生物標誌物的行列。目前已有多種技術平台被應用於生物標誌物研究,如包括基因組學、蛋白質組學、肽組學、代謝組學等在內的組學平台,以及包括納米技術、生物信息學、抗體芯片、高內涵篩選技術、無標記相互作用分析技術等多種前沿技術在內的手段與方法,都為快速獲得及篩選生物標誌物帶來了極大的可能。
❖ 診斷性生物標誌物:用於檢測或確認疾病狀態,或識別不同疾病亞型。
❖ 預後性生物標誌物:反映疾病預後特征、疾病複發或進展風險。
❖ 預測性生物標誌物:用於預測患者對某種治療或幹預措施可能產生某種療效應答。
❖ 藥效學生物標誌物:反映患者在接受治療後產生某種生物學應答。
❖ 安全性生物標誌物:用藥前或用藥過程中監測從而避免或降低患者發生不良反應。
❖ 監測性生物標誌物:監測疾病狀態變化(如複發等)。
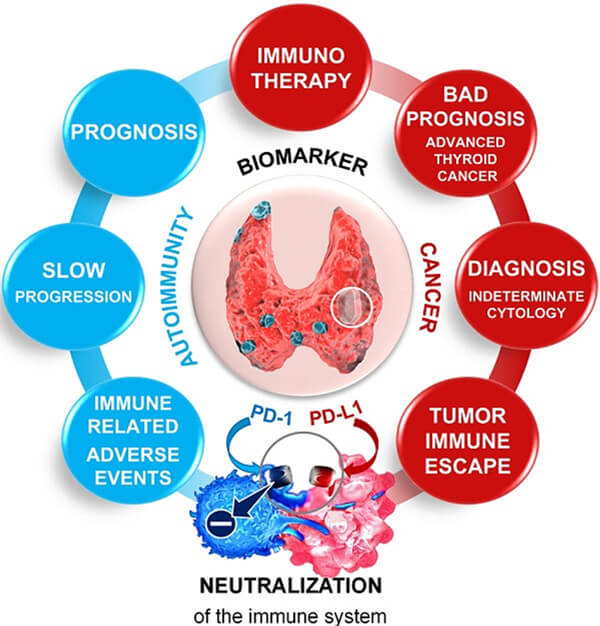
❖ PD1/PD-L1
❖ ErbB2/HER2
❖ p-FGFR1/FGFR2/FGFR3、p-ERK、p-CREB、p-AKT
❖ EGFR
❖ VEGF
❖ p53
❖ Cyclin D1
❖ COX-2
❖ Cytokeratin 7(CK7)
❖ K-Ras
❖ SOX2
❖ MET
❖ Fas
❖ ER-α
❖ Ki-67等
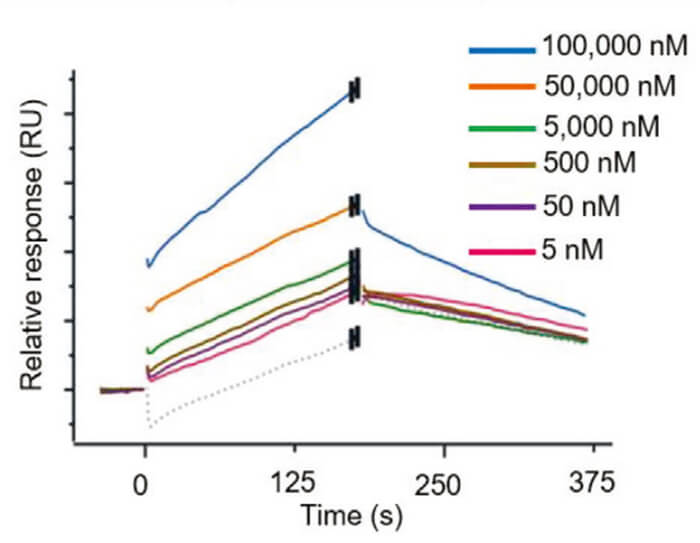
WBC100 是一種新型口服有效的分子膠,可選擇性地降解 c-Myc 蛋白而對其他蛋白無作用活性,並有效殺死c-Myc過表達的癌細胞。SPR結果顯示 WBC100 與 c-Myc 蛋白結合,且存在劑量依賴性。此SPR實驗正是通過hjc黄金城使用Biacore T200儀器進行的。
Surface plasmon resonance (SPR)[2]
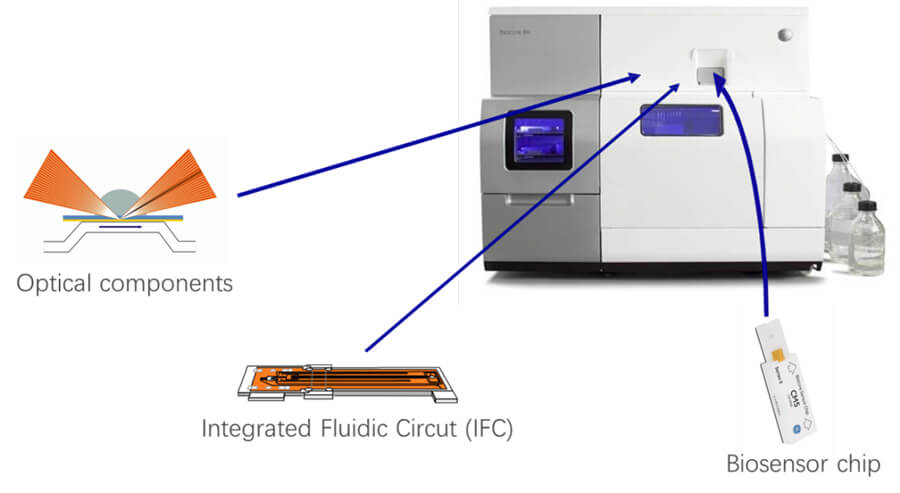
❖ 8 needles and 16 flowcells, study 8 targets at the same time;
❖ High-throughput, 500 compounds/day;
❖ Fast detection speed,finish one affinity and kinetic test in 2-15 minutes.
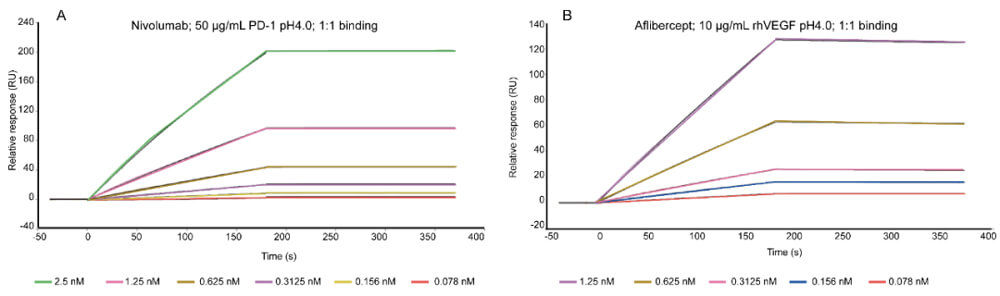
A: Binding kinetics of different doses of Nivolumab with PD-1 (Biacore 8K)
B: Binding kinetics of different doses of Aflibercept with recombinant human VEGF (Biacore 8K)
hjc黄金城生物分析部可以為客戶提供小分子藥物、大分子生物製品、生物標誌物的篩選與開發,以及臨床前和臨床階段的研究服務。可以提供符合FDA/NMPA GLP的生物技術藥物生物分析服務,以支持蛋白藥物、抗體藥物、疫苗、生物標誌物、細胞和基因治療藥物的早期開發,及其臨床前研究和臨床研究。
❖ 免疫分析方法的開發及方法學驗證
❖ 蛋白、抗體、ADC、多肽藥物、核酸、疫苗及細胞與基因治療產品等的分析
❖ 生物標誌物的篩選、驗證與分析、細胞因子檢測
❖ 抗藥性抗體(ADA)免疫原性分析
❖ 疫苗的免疫原性分析
❖ 病毒的活性分析
❖ 疫苗的效價測定
❖ 臨床樣品生物分析
❖ 支持PK 藥代動力學、TK 毒代動力學、組織分布試驗、IND申報
❖ 實驗室實行全麵的信息化管理,運用驗證過的實驗室信息管理係統(Watson LIMS 7.2)建立了完善的樣品管理鏈和實驗數據的處理、跟蹤與存儲鏈;
❖ SensaTronics溫度監控係統;
❖ 驗證過的WinNonlin 軟件用於數據分析;
❖ 數據被FDA和NMPA接受,提供全麵符合FDA/NMPA/OECD GLP規範要求的生物技術藥物分析服務;
❖ 獨立的小分子生物分析平台和生物技術藥分析平台;
❖擁有SpectraMaxM4/M5/i3x, MSD, Luminex, Biacore 8K, Envision,Gyrolab,ABI7500 qPCR、ddPCR、FACS等全方位多功能的技術平台;
❖ 靈活運用ELISA,ECL,IP,Co-IP,qPCR,ddPCR、FACS,Elispot、酶學、Cell-based 等多種方法,支持前沿生物藥,種類包括蛋白、抗體、ADC、多肽、核酸、疫苗及細胞基因治療藥物的早期開發,及其臨床前研究和臨床研究;
❖ 開發並驗證針對近百個不同靶點,如CD-4,CTLA-4,PD-1,PD-L1及T-DM1類似物ADC等的分析方法,支持PK/TK/免疫原性(Total ADA, Nab)/生物標誌物/細胞因子等分析。

往期文章中,我們通過從FACS 檢測 Cytokine 檢測和細胞功能檢測多個實際案例的角度出發,詳細介紹了“hjc黄金城流式細胞技術平台”(點擊了解)。截至目前,hjc黄金城承接的流式檢測項目已經近400項,包括細胞表麵抗原表達的流式檢測;細胞增殖、細胞分化、細胞凋亡等的流式分析;動物外周血及各免疫器官檢測;移植瘤模型流式檢測等。hjc黄金城流式檢測團隊將每一個案例的特點與多年實戰經驗和技術積累相結合,謹慎地將優質實驗結果提交到客戶手上,持續助力客戶的研發項目獲批。
免疫組化,也稱免疫組織化學技術(immunohistochemistry)或免疫細胞化學技術(immunocytochemistry)。是指應用免疫學基本原理即抗原與抗體特異性結合的原理,通過化學反應使標記抗體的顯色劑顯色來確定組織細胞內抗原(多肽和蛋白質),對其進行定位、定性及相對定量的研究。根據抗原抗體反應和化學顯色的原理,組織切片或細胞樣本中的抗原先和一抗結合,再利用一抗與二抗反應,DAB進行顯色,進而進行分析。
❖ 組織處理、固定、切片
❖ 抗原修複
❖ 除去內源性過氧化物酶
❖ 封閉
❖ 一抗、二抗孵育
❖ 檢測
❖ 複染
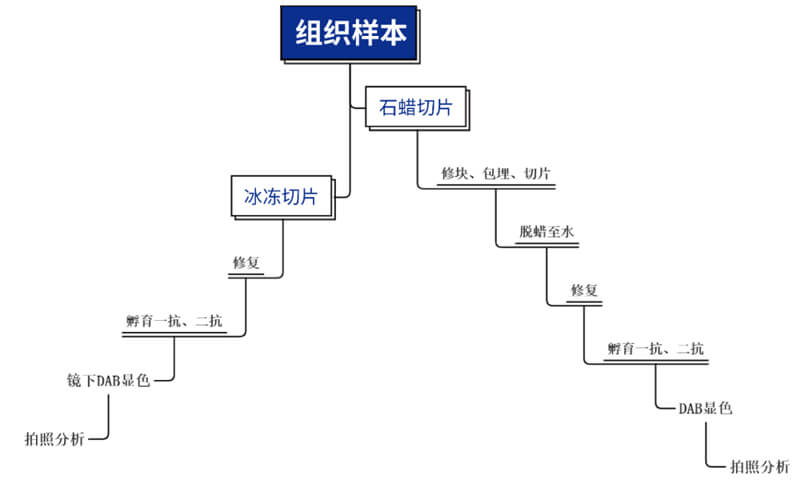
組織固定可保存抗原,防止采集的組織自溶和壞死。組織包埋可在切片過程中對組織提供支撐,使切片更堅實。
| 石蠟切片 | 冰凍切片 | |
| 固定 | 包埋前:甲醛 | 切片前或切片後:甲醛、甲醇、乙醇或丙酮 |
| 切片 | 切片機 | 冰凍切片機 |
| 儲存 | 室溫下儲存多年 | -80 °C下儲存1年 (-190°C下儲存時間更長) |
| 優勢 | 容易操作,不會損壞切片 | ♦ 保留酶的功能和抗原性 ♦ 實驗流程簡短(通常不需要冗長的固定步驟) |
| 局限性 | ♦ 過度固定會掩蓋抗原表位,進而增加抗原修複的需求 ♦ 處理時間長:在梯度酒精和二甲苯中逐步脫水,以便於石蠟滲透。 | ♦ 如果沒有快速冷凍組織”可能會形成冰晶,從而破壞組織結構 ♦ 冰凍切片通常比石蠟切片厚,可能會導致分辨率低、圖像差 ♦ 可能需要阻斷內源活性酶。 |
石蠟切片 vs冰凍切片
對甲醛固定的組織切片進行抗原修複,以暴露抗原位點,從而使抗體結合。
| 熱誘導的抗原表位修複 | 蛋白水解酶誘導的抗原表位修複 | |
| 優勢 | 抗原表位的修複更溫和,參數更可控。 | 適用於較難修複的抗原表位。 |
| ph值 | 通常使用pH6的緩衝液,但堿性緩衝液也在廣泛使用。必須通過實驗確定 | pH值通常為7.4。 |
| 溫度 | 約95°C。 | 通常為37°C |
| 孵育時間 | 10-20分鍾 | 10-15分鍾 |
| 緩衝液組分 | 取決於靶抗原所需的pH 值。常用的緩衝液包括檸檬酸鈉、EDTA和Tris-EDTA | 酶(如胃蛋白酶、蛋白酶K 或胰蛋白酶)的中性緩衝液。 |
| 注意事項 | 微波爐加熱可能會導致抗原修複不均勻。劇烈沸騰會導致脫片(組織與載玻片分離)。 | 酶修複有時會破壞切片的形態- 濃度和時間需要優化 |
抗原修複的主要方法
用血清或BSA封閉,防止抗體的非特異性結合,並降低背景和潛在的假陽性結果。
❖ 蛋白封閉:使用血清或BSA 進行封閉對於防止抗體與組織或Fc 受體(與抗體恒定區(Fc)結合的受體)發生非特異性結合至關重要。二抗種屬來源的血清是很好的封閉試劑。使用牛血清白蛋白(BSA)或酪蛋白,可用於阻斷非特異性抗體結合。
❖ 生物素封閉:在使用基於親和素/生物素的檢測係統時,阻斷內源性生物素,因為內源性生物素存在於許多組織中,特別是腎髒、脾髒、肝髒和大腦中。用親和素與組織孵育,阻斷內源生物素,然後用外源生物素孵育,以阻斷親和素分子上額外的生物素結合位點。
用血清或BSA封閉,防止抗體的非特異性結合,並降低背景和潛在的假陽性結果。
❖ 酶顯色法:顯色檢測使用酶能夠催化可溶性底物產生有色沉澱。這些酶通常偶聯在二抗上,也可以偶聯在一抗上用於直接檢測。最常用的酶有HRP 和AP,前者將DAB 轉化成棕色產物,後者將3-氨基-9-乙基哢唑 (AEC) 轉化成紅色產物。顯色檢測通常比熒光檢測更靈敏。此外,不同於熒光染料,有色沉澱物有光穩定性,因此染色切片能夠保存多年。熒光檢測需要使用專業熒光顯微鏡和濾光片,顯色檢測僅需使用標準顯微鏡。然而,顯色檢測的孵育和封閉步驟比熒光法更多,時間也更長。
❖ 熒光法:熒光檢測(免疫熒光)是基於熒光基團被特定波長的光激發後發射波長較長的熒光的特性。熒光檢測常常用於需要同時檢測多種抗原的情況。熒光染料可以與一抗或二抗直接偶聯,也可與鏈黴素親和素偶聯。
儀器設備(部分舉例)
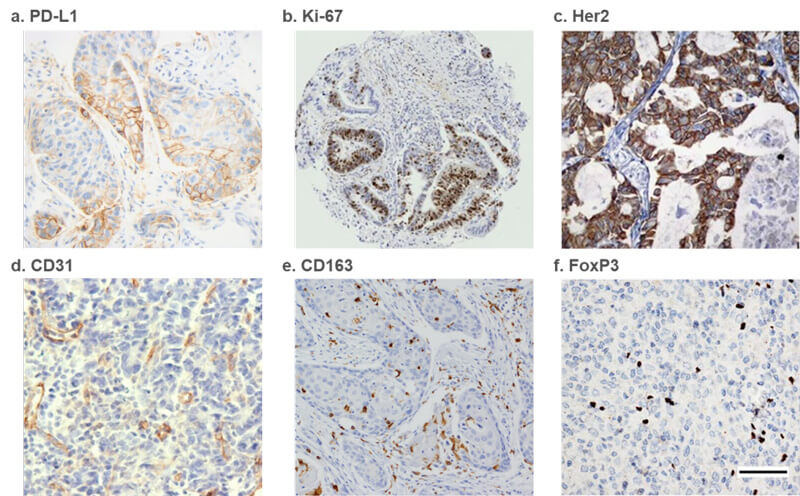
IHC Analysis of the expression of a)PD-L1 from lung adenocarcinoma[3]; b)Ki-67 from periampullary tumors[4]; c)Her2 from lung tumor[5]; d)CD31 from human gastric adenocarcinoma[6]; e)CD163 (M2 TAM marker) from oral squamous cell carcinoma (OSCC)[7]; f)FoxP3 from human glioblastoma[8].
基於基因組學、蛋白組學、細胞組學及病理組學等綜合性轉化醫學平台;高質量的研發管理團隊;hjc黄金城轉化醫學平台致力於為全球合作夥伴提供全方位生物標誌物發現、靶點驗證、伴隨診斷開發與商業化檢測等一體化解決方案。
❖ 以ELISA、ECL(MSD), SIMOA(HD-X), Biacore 8K 技術構建的的蛋白質相互作用,蛋白水平生物標誌物平台;
❖ 以流式細胞術(BD Symphony A3,BD Fortesssa, Beckman CytoFLEX S)為主構建的細胞水平生物標誌物平台;
❖ 以熒光定量PCR技術構建的多重核酸水平生物標誌物平台;
❖ 免疫組化(TAMs-IHC,FISH)技術構建的病理水平生物標誌物平台等;
致力於解決創新藥物的研發難點,助力精準醫療!
我們很幸運地生活在一個生物醫學科學看似無限可能的時代。在這個時代,研究的問題不再主要受技術能力的限製。轉化醫學的實現需要同樣持續大膽的願景和執行。在過去幾十年,轉化醫學取得了顯著進步,未來轉化醫學將繼續發展,並更快、更高效地為更多患者提供更多治療的可能性!
[1] Hugues Dolgos, et al. Translational Medicine Guide transforms drug development processes: the recent Merck experience. Drug Discov Today. 2016 Mar;21(3):517-26. doi: 10.1016/j.drudis.2016.01.003.
[2] Ying Xu, et al. A Selective Small-Molecule c-Myc Degrader Potently Regresses Lethal c-Myc Overexpressing Tumors. Adv Sci (Weinh). 2022 Mar;9(8):e2104344. doi: 10.1002/advs.202104344.
[3] Jonas J Heymann, et al. PD-L1 expression in non-small cell lung carcinoma: Comparison among cytology, small biopsy, and surgical resection specimens. Cancer Cytopathol. 2017 Dec;125(12):896-907. doi: 10.1002/cncy.21937.
[4] Mark M Aloysius, et al. Predictive value of tumor proliferative indices in periampullary cancers: Ki-67, mitotic activity index (MI) and volume corrected mitotic index (M/V) using tissue microarrays. World J Surg. 2010 Sep;34(9):2115-21. doi: 10.1007/s00268-010-0681-3.
[5] Montse Verdu, et al. Cross-reactivity of EGFR mutation-specific immunohistochemistry assay in HER2-positive tumors. Appl Immunohistochem Mol Morphol. 2015 Sep;23(8):565-70.
[6] Qingling Wang, et al. EPCR promotes MGC803 human gastric cancer cell tumor angiogenesis in vitro through activating ERK1/2 and AKT in a PAR1-dependent manner. Oncol Lett. 2018 Aug;16(2):1565-1570. doi: 10.3892/ol.2018.8869.
[7] Faustino J Suárez-Sánchez, et al. Macrophages in Oral Carcinomas: Relationship with Cancer Stem Cell Markers and PD-L1 Expression. Cancers (Basel) (IF: 6.13; Q1). 2020 Jul 2;12(7):1764. doi: 10.3390/cancers12071764.
[8] Qi Yue, et al. The prognostic value of Foxp3+ tumor-infiltrating lymphocytes in patients with glioblastoma. J Neurooncol. 2014 Jan;116(2):251-9. doi: 10.1007/s11060-013-1314-0. Epub 2013 Nov 26.[9] Christopher P Austin.Opportunities and challenges in translational science. Clin Transl Sci. 2021 Sep;14(5):1629-1647. doi: 10.1111/cts.13055.
 相關新聞
相關新聞