2010-2014年,國家食品藥品監督管理總局批準的中藥新藥治療領域主要集中於心腦血管、呼吸係統以及泌尿生殖係統;從審評周期來看,婦科、呼吸係統和泌尿生殖係統藥物平均申報周期較短;從批準率來看,泌尿生殖係統、兒科為批準率較高的2個領域。由此推斷心腦血管係統是中藥研發的經典領域;泌尿生殖係統、兒科和婦科為中藥新藥研發較有前景的領域。
中藥新藥研發應符合中醫藥理論是《藥品注冊管理辦法》對中藥新藥研發立項依據和立題的基本要求。《2013年國家食品藥品監督管理局審評中心年報》顯示,2013年僅有15種中藥新藥品種獲得批準文號。自2010年起,每年獲批的中藥新藥製劑品種平均數量為 13.4 種,而平均每年申請中藥新藥生產的數量為 35.6 種,批準率為 37.6%。麵對如此嚴格的審批要求,新藥研發單位應明確研發方向以降低新藥研發風險。
數據來源與研究方法:數據來源於 CFDA 和 CDE 官方網站。收集 2008-2014 年 CFDA、CDE 受理、批準生產的中藥新藥品種,使用 Excel 對數據進行篩選、排序、計算等統計分析工作。
2008-2013年 CFDA受審的中藥新藥生產申請數量
由圖 1 可以看出,《藥品注冊管理辦法》2007版(以下簡稱新版管理辦法)以及中藥相關管理規定實施後,仿製藥申請和簡單改劑型等申請數量大幅減少,導致 2008 和 2009 年申報中藥生產數量急劇下降。這一現象說明新版管理辦法通過提高藥品注冊申報要求,規範藥品審評審批程序、縮短新藥審評時間以及延長仿製藥、改劑型審評時間等措施,在一定程度上遏製了藥品研製不規範和低水平重複的行為。
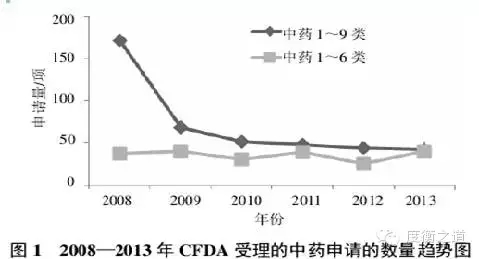
2008-2013 年,CDE 共受理的中藥新藥生產申請數量分別為 37、40、30、39、25、40 項,共 211項。新版管理辦法中規定,中藥注冊分類 1~6 的品種為新藥,注冊分類 7、8按新藥申請程序申報。從圖1中還可看出,這幾年間受審的中藥 1~6 類數量較平穩,呈小幅波動狀態。
CFDA 批準中藥新藥的狀況分析
2010-2014 年 CFDA 批準生產的中藥新藥製劑品種數量分別為 11、17、16、14、9 種,共67 種。
1、批準中藥新藥的治療領域分布
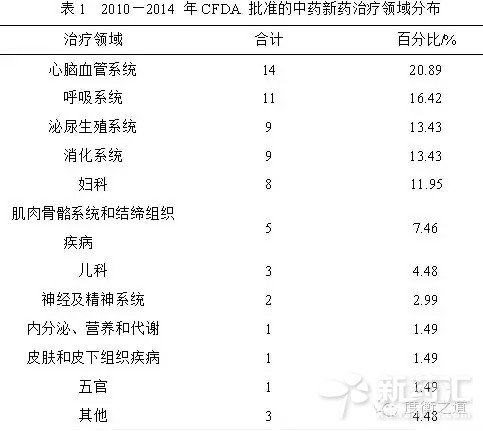
根 據 ICD-10( TheInternational Statistical Classification of Diseases and Related HealthProblems 10th Revision,國際疾病傷害及死因分類標準第 10版)的疾病分類標準(共 22類),再結合中醫中藥治療疾病分類,對批準的 67種新藥的治療領域進行分類,結果見表 1。
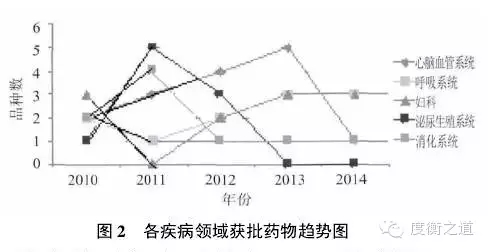 2、各治療領域藥物申報周期
2、各治療領域藥物申報周期
根據CDE對每個品種承辦日期(CDE開始承辦所報品種的技術審評工作時間)和審批日期(CFDA批準日期),計算前 5 大治療領域品種的平均申報周期,結果見表 2。婦科和呼吸係統為最快獲得批準的治療領域,婦科平均為31.50個月(約2.6年);其次是呼吸係統,為 48.32 個月(約 4 年);其他領域藥物均在遞交申請後,經過51.02~62.65個月(4~6 年)獲得批準生產。而批準生產數量最多的心腦血管藥物所需時間最長,是最短申報周期的近2倍。

3、各治療領域的主要疾病
通過分析發現,各治療領域內的新產品適應症比較集中,故進一步細分各治療領域適應症,統計結果見表 3。
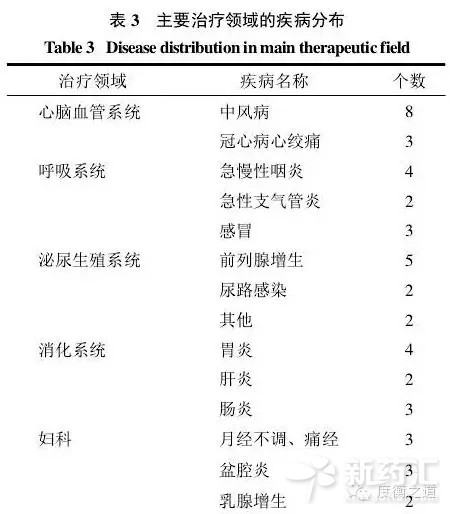
在心腦血管領域,治療中風病的藥物獲批最多,多以用於中風病(輕中度腦梗死)恢複期氣虛血瘀證和痰瘀阻絡證為主。其中以氣虛血瘀證為最多,如5類中藥龍血通絡膠囊,臨床主要用於中風病經絡恢複期血瘀證,治療血瘀引起的中風。治療中風病獲批的這8個品種中有4個品種為中藥6類,2個5類中藥(銀杏二萜酯葡胺注射液、龍血通絡膠囊),1個為較少申報的中藥 6.2 類(益氣通絡顆粒)。
在消化係統領域,獲批的藥物主要集中於治療胃腸道疾病,其中以單純用於緩解胃部不適症狀的藥物居多。如中藥 6 類良附軟膠囊,具有溫胃理氣的功效,用於寒凝氣滯、脘痛吐酸、胸腹脹滿等症。
在婦科領域,獲批的中藥主要以治療盆腔炎和乳腺增生疾病為主,其中治療盆腔炎的品種為3個,均為治療慢性盆腔炎中醫辨證屬濕熱內蘊證的藥物。這一適應症的藥物也與慢性盆腔炎以濕熱型居多相適應。治療乳腺增生的藥物為2個,均以疏肝行氣、活血化瘀的方法治療辨證屬肝邪氣滯型乳腺增生病。
在泌尿生殖領域,主要藥物集中於前列腺疾病,如良性前列腺增生和慢性非細菌性前列腺炎的血瘀濕阻證。
結合中藥新藥申報情況的深入分析
數據顯示,2008—2013年,申請注冊的中藥新藥品種在治療領域分布上主要集中於精神神經、呼吸、婦科、消化及心腦血管等領域,所占比例達58.77%,而兒科、皮膚等領域的新藥注冊申請數量較少。結果見表4。

結合表1和表4,神經及精神係統疾病用藥物,從申請情況來看,2008—2013 年共有 83 項申請,但 2010—2014 這5 年間,僅在 2012、2013 年,批準2個治療抑鬱症的藥物,以及 1個治療輕中度阿爾茨海默病的補充申請,“申報多,批準少”成為神經及精神係統藥物的主要特點,治療疾病較單一,僅為抑鬱症、阿爾茨海默病的藥物。
泌尿生殖係統疾病用藥,從 2010—2014 年共批準 9 種藥物上市,但 2013、2014 年均無批準藥物。除臨床療效影響批準結果外,近些年申請注冊的藥物僅為 26 個,可供篩選的新藥申請數量較少也是一個重要因素。泌尿生殖係統藥物批準率較高,高達34.1%,前列腺增生和尿路感染疾病藥物為主要批準治療領域。同時,由於泌尿生殖係統疾病的種類、適應症較多,批準率高,故應該關注該領域中藥新藥的研發。
兒科和心腦血管疾病的批準率均較高,達到25%左右。心腦血管係統藥物自 2010 年批準上市的數量逐漸增長,而 2014年僅有 1 種藥物獲批。心腦血管藥物市場逐漸飽和,已接近滿足臨床需求。近些年,兒科用藥僅有 12個中藥新藥申請,但已有 3 個品種獲批生產,批準率較高。兒童(0~14歲)相較於成年人,不論是其身體髒器、新陳代謝率,包括用藥習慣和劑量都有其特點。中成藥為臨床兒科常用的一線藥物,具有保健、調理身體機能的作用,與化學藥單一成分的治療相比,有著副作用小等優勢。從兒童用藥數量來看,目前,我國兒童中藥製劑仍處於匱乏狀態,兒童用中成藥僅占新研製的中成藥的 6%,在整個中藥製劑品種中比例不足 2%,亟需相關的藥物開發。
近些年,中藥注冊申請主要以申請新藥為主,特別是中藥 6 類的申請,僅 2008—2013 年 CDE 審評的 604 個中藥新藥注冊申請中,注冊分類第 6 類(新的中藥、天然藥物複方製劑)的品種數量最多,占到全部中藥新藥注冊申請的85.76%。心腦血管、呼吸係統、消化係統是中藥新藥批準率高的主要疾病領域,占到整體的 50.7%。
從2010-2014年CDE批準的中藥新藥的治療領域的適應症來看,中風病、前列腺疾病、胃腸道疾病、咽炎、月經不調等疾病是目前預期前景看好的領域,並且仍然是未來中藥新藥研發中關注的熱點領域。另外,從申報周期來看,婦科、呼吸係統疾病以及泌尿生殖係統疾病為獲批最快的 3 個治療領域。婦科疾病藥物作為審批最快的品種,平均申報周期為 2.6 年。對於婦女月經不調及經前期、更年期綜合征等疾病,西醫往往采用激素療法,易複發,而中醫采取整體調理方法,療效確切,故應多加關注;泌尿生殖係統申報周期為 4.25 年,並且根據這些年的批準情況來看,泌尿生殖係統的批準率較高,前列腺增生和尿路感染為批準較多的適應症,值得多加關注。




















 相關新聞
相關新聞