國家優先審評這17個藥品!曝出一個最大熱門
9月14日,國家藥審中心將17個藥品納入優先審評的名單,此次被列入優先審評品種名單涵蓋較廣,有罕見病、兒童用藥、重大疾病(抗艾滋病用藥),還有現有治療手段相比具有明顯治療優勢的創新藥和增加新的適應症以及仿製藥。
獲優先審批5大理由
和創新藥等相比,仿製藥在安全性等方麵不存在問題的,所以,從現在審評來講,隻要能夠和原研藥有同樣的質量水平,應該就可以過關,所以被列入優先審評後,預計其獲批速度將大大加快,那麽,被列入優先審評的依據在哪裏呢?
從國家藥審中心後麵所列的理由主要有下麵5個:
按與原研藥質量和療效一致的標準完善後重新申報的首家報產品種
歐盟已批準上市
已在歐盟遞交注冊申請,獲得英國MHRA GMP認證
同步遞交美國ANDA申請,已通過FDA現場檢查
同步遞交歐盟注冊申請,已通過歐盟GMP檢查
從上麵5個的理由來看,一個是藥品要有國際範,通過了FDA、歐盟、英國各種認證;另外一個是按與原研藥質量和療效一致的標準完善後重新申報的首家報產品種。
最受熱捧的品種終於要殺出一個勝者了
此次隻有一個品種,布洛芬注射液獲得這張優先權。
布洛芬是一個非常火的品種,在中國家喻戶曉的芬必得就是布洛芬緩釋膠囊。作為非甾體類抗炎藥,雖然有胃腸道不良反應,但其口服固體製劑的市場經久不衰。
2009年6月,布洛芬的新給藥途徑的布洛芬注射液在國外成功上市,Cumberland公司的布洛芬注射液在美國獲得FDA的上市許可,商品名:Caldolor,這是布洛芬的首個注射製劑,為疼痛和發熱、同時又不方便口服的患者帶來了方便。
如此“老藥”又長出了“嫩芽”,這一劑型,引起國內企業紛紛追逐該品的研發,其熱度一浪高過一浪,信狐藥訊的數據查詢結果顯示,目前有60多家藥企在拚搶這個的品種,其中有62家申報臨床,隻有2家申報生產。
此次獲得優先審批權的成都苑東生物製藥股份有限公司,其申報生產的時間為2016年8月1日。在申報生產階段獲得優先審評,其上市速度無疑是會大大加快,尤其這還是按與原研藥質量和療效一致的標準完善後重新申報的,其市場意義就更大。對於企業迅速搶占市場來說,無疑占據了相當大的優勢。
第二家申報生產的企業為9月23日,雖然申報時間隻晚了一個半月,但是其上市時間相差估計不會有1個半月,短短幾天喪失了市場先機。
畢竟要走國際化這條道路不是每家企業的追求,但是像成都苑東生物製藥股份有限公司這樣,迅速調整,按照新的標準,快速申報,反而能搶到一定的先機。尤其是國家臨床試驗核查後,那麽多品種被打倒了。此時,如果按照新的標準,速度申報,很有可能會被列入優先審評名單的,獲得市場的先發權。
對於積極尋找好品種的市場人員來講,也可以根據研發動態積極遴選新的品種。
現在進入賽柏藍微信平台後,點擊頁麵右下角的數據查詢功能,可以通過微信查詢熱點品種的注冊現狀,同時還可以利用訂閱跟蹤功能,及時獲取該品種的注冊受理最新進展,預知上市日程,搶得先機。
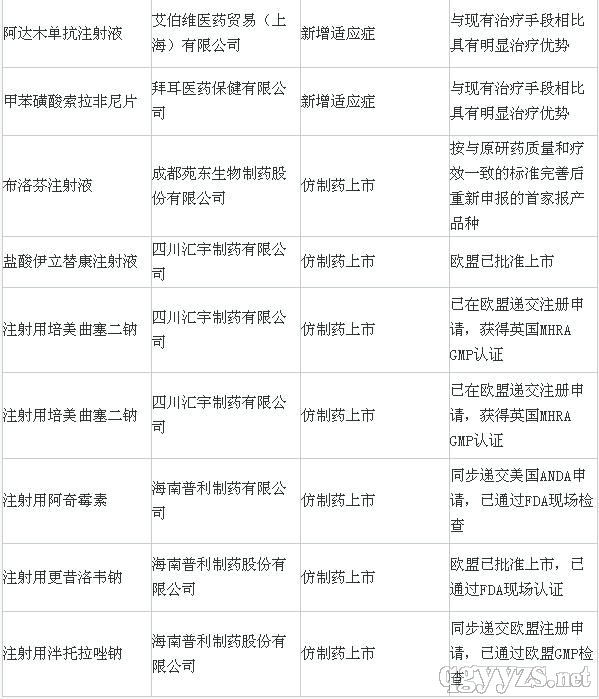
附:獲得優先審評的品種名單

分享到:















 相關新聞
相關新聞