
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




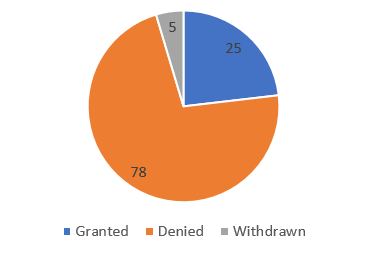
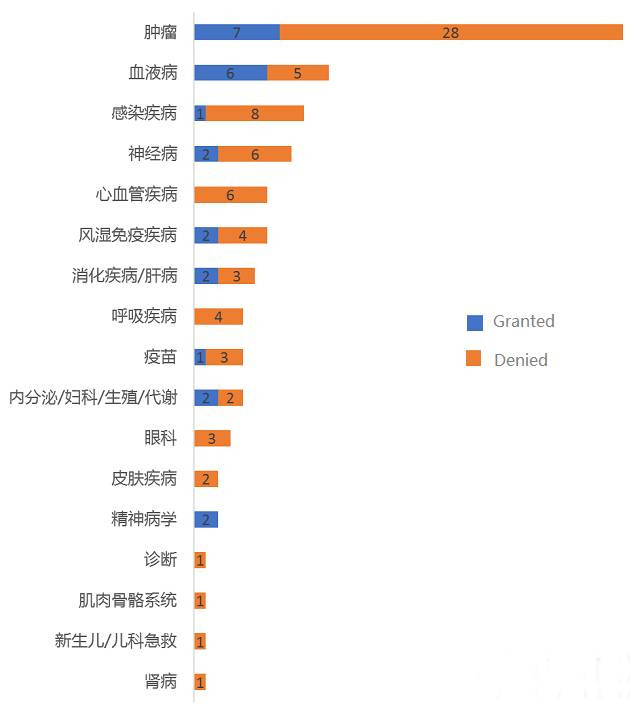
5月24日,EMA最新公布了5款獲得認定的“優先藥物”,比較值得一提的是治療膠質母細胞瘤的APG101。膠質母細胞瘤是最常見的惡性腦部腫瘤,治療後複發概率高,5年生存率低於35%。
EMA 5月24日授予優先藥物認定的5款新藥
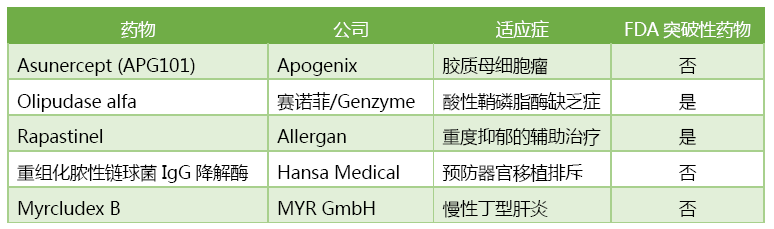
APG101是一款由總部位於德國海德堡的Apogenix公司開發的腫瘤免疫治療藥物,是由CD95受體胞外結構域和IgG1抗體Fc段組成的全人源融合蛋白,可以與腫瘤細胞表麵的CD95結合,阻斷腫瘤細胞生長。在一項納入86例複發性膠質母細胞瘤患者的II期研究中,APG101可顯著延長患者生存期,EMA由此授予了APG101“優先藥物”資格。EMA正是基於這項研究授予了APG101“優先藥物”資格。
獲得“優先藥物”認定後,Apogenix公司可以與EMA有更早期的密切接觸,獲得臨床試驗設計的優化意見,有利於獲得高質量的研究數據,也有利於讓這款臨床急需的藥物早日上市以造福患者。
 相關新聞
相關新聞