
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




AXL酪氨酸激酶的過度表達或激活與炎症的發生、發展以及腫瘤的侵襲、轉移等過程密切相關。然而,針對AXL的研究直到近年來才受到廣泛的關注。2013年首個AXL抑製劑進入臨床試驗,成為AXL作為抗癌靶點的一個重要裏程碑。Istvan Szabadkai等人[1]最近提出了一個新的小分子化合物21f,描述了其結構、合成和生物活性,並證實是一種選擇性的AXL酪氨酸激酶抑製劑。在未觀察到毒性的情況下,在人類乳腺癌異種移植模型中,使用21f後局部腫瘤停滯生長的幾率達到40%,這表明21f具有成藥的可能性,值得進一步的具體研究和探索。
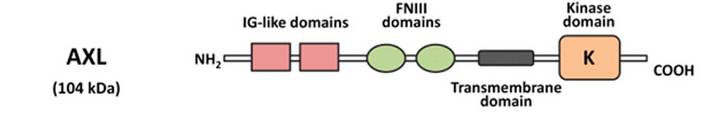
AXL靶點概括
受體酪氨酸激酶(RTKs)是連接細胞外和細胞內環境的跨膜蛋白。作為信號轉導的調停者,其在正常的細胞過程中扮演了重要的角色,包括分化、粘附、遷移、凋亡、代謝。哺乳動物的受體酪氨酸激酶中有一個亞科稱為TAM家族,包括AXL、MER和TYRO-3。AXL激酶的過表達最初是在慢性粒細胞白血病和慢性骨髓增生症中發現的。隨後,Paccez等人發現在乳腺癌、肺癌、前列腺癌、結腸癌、食管癌、肝癌等多種癌症中也存在AXL激酶過表達。
AXL受體酪氨酸激酶是由胞外區、跨膜區和胞內區組成,屬於Ⅰ型跨膜單鏈。其胞外配體結合區域由兩個免疫球蛋白的結構域和兩個纖維蛋白的重複序列相連而成;胞內段是酪氨酸蛋白激酶的催化部位,具有自身磷酸化的特點。胞外段則通過一個a螺旋跨膜結構與胞內的酪氨酸激酶相連。
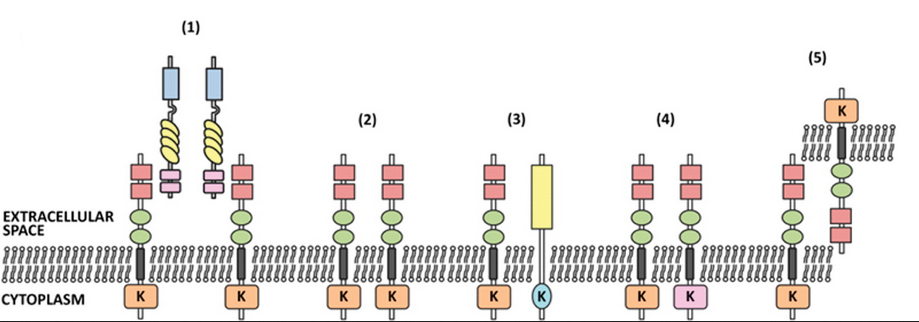
AXL可以被多種機製激活,活化方式具體有:(1)AXL與GAS6配體依賴性活化;(2) AXL的配體獨立活化;(3)非TAM家族蛋白對AXL的異源激活;(4) MER或TYRO3對AXL的異源激活;(5) AXL的胞外配體獨立活化。最常見的是配體依賴性激活,其中AXL與GAS6結合,形成由兩個AXL分子與兩個GAS6分子結合的二聚體複合物。其他的激活機製也可能會發生,如當AXL被過度表達或在氧化應激下,往往會發生配體獨立激活[2];以及在B細胞慢性淋巴細胞白血病中發現AXL和TYRO3的二聚化[3]。
AXL抑製劑的研究現狀
已有研究發現,TAM信號轉導在凋亡細胞的清除、固有免疫以及炎症調節反應中起著重要的作用。TAM的信號缺陷可以導致凋亡細胞清除障礙以及固有免疫反應中炎症的無限製級聯放大。因此,通過抑製TAM信號轉導,可以達到治療癌症和緩解免疫抑製的效果,並能治療晚期敗血性休克。
近來的研究顯示,激活的AXL會幫助癌細胞發展出對厄洛替尼的耐藥性,而在細胞中抑製AXL活性,則能恢複細胞對厄洛替尼的敏感性。若將AXL抑製劑和厄洛替尼組合使用則能夠實現優勢互補。一方麵,激酶抑製劑能夠快速抑製腫瘤細胞,並增強頑固腫瘤對厄洛替尼的敏感性;另一方麵厄洛替尼能夠幫助激酶抑製劑發揮持久的抗腫瘤作用。此外激酶抑製劑還能夠協助活化T細胞來清除腫瘤細胞。BerGenBio就基於上述觀點,專注開發AXL激酶抑製劑,試圖將其發展成癌症治療中聯合用藥的基石之一。下圖為已報道的對AXL有活性的小分子酪氨酸激酶抑製劑。
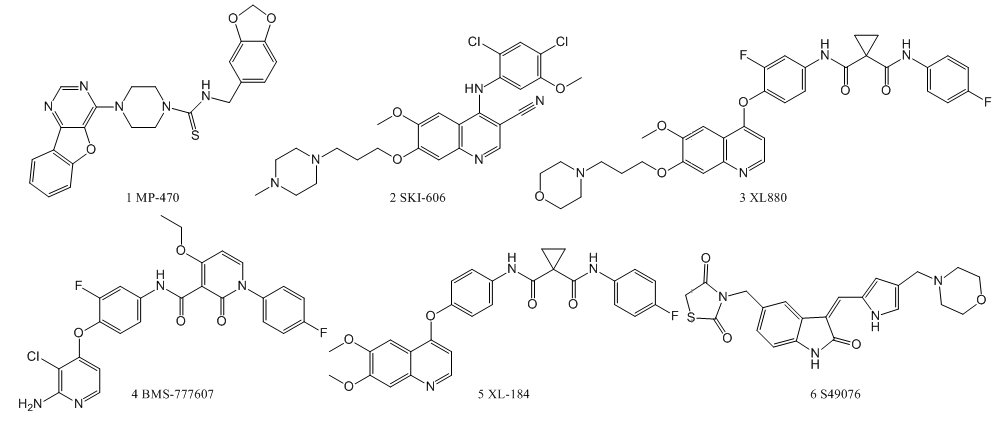
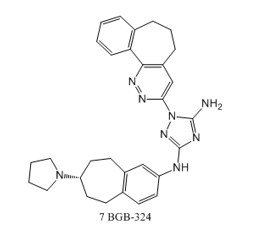
然而,上述小分子激酶抑製劑的起始目標靶點並不是AXL,第一個針對AXL激酶的選擇性抑製劑是化合物R428(BGB-324)(7) [4]。其作用機製是抑製AXL的磷酸化,打破膜上AXL激酶的穩態調控,從而下調AXL膜上的表達量。BGB-324是BerGenBio公司研發的同類首創、高選擇性、生物可用的口服AXL小分子抑製劑。
AXL在不同實體和癌症的生存、擴散和耐藥機製中的突出作用,都表明AXL抑製作為一種抗癌藥物,特別是針對晚期疾病,值得期許。目前針對AXL的各種候選藥物正在臨床研究中,預計會有更多的藥物問世,可以為癌症患者提供新的治療方案。
參考文獻:
1, Istvá̈ri,́̈ AxelChoidas, Axel Ullrich and László̋r−6292.
2, Heiring, C. Dahlback, B. Muller, Y. A.Ligand recognition and homophilic interactions in Tyro3: structural insightsinto the Axl/Tyro3 receptor tyrosine kinase family J. Biol. Chem. 2004, 279,6952-6958.
3, Sinha, S. Boysen, J. Nelson, M.;Secreto, C. Warner, S. L. Bearss, D. J. Lesnick, C. Shanafelt, T. D. Kay,N. E. Ghosh, A. K. Targeted Axl inhibition primes Chronic Lymphocytic LeukemiaB cells to apoptosis and shows synergistic/additive effects in combination withBTK inhibitors Clin. Cancer Res. 2015, 21, 2115-2126.
4, Holland, S. J. Pan,A. Franci, C. Hu, Y. Chang, B. Li, W. Duan, M. Torneros, A. Yu, J. Heckrodt, T. J. Zhang, J. Ding, P. Apatira, A.; Chua, J. Brandt, R. Pine,P. Goff, D. Singh, R. Payan,D. G. Hitoshi, Y. R428,a selective small molecule inhibitor of AXL kinase, blocks tumor spread andprolongs survival in models of metastatic breast cancer. Cancer Res. 2010, 70,1544−1554.
 相關新聞
相關新聞