各種眼科疾病隨著老齡化逐漸增加,而近年來,眼科疾病的發病率逐漸年輕化,相關眼科用藥市場需求也在不斷蓬勃發展!近期,受疫情影響居家隔離期間,我們日常電子產品的使用時間增加,用眼負擔加重,容易出現眼睛幹澀、疼痛、視物模糊等症狀,小編溫馨提醒您:保持健康護眼的習慣,科學用眼,美好無限!
hjc黄金城臨床前眼科研究平台集合了先進的給藥技術和分析手段,精良的儀器設備以及經驗豐富的研發團隊,為存在眼科藥物開發需求的客戶提供優質高效的試驗研究服務以及專業的注冊申報支持和項目管理服務。
眼部疾病
眼睛是一個球狀結構器官,由前段和後段兩個主要部分組成。血眼屏障包括血房水屏障和血視網膜屏障,保護眼睛免受異物的傷害。眼科是研究發生在視覺係統,包括眼球及與其相關聯的組織有關疾病的學科。眼部疾病包括各種眼前節疾病和眼後節疾病。眼前節疾病包括:角膜損傷、幹眼症、角膜炎、結膜炎和白內障等。眼後節疾病最常見於視網膜和脈絡膜。包括年齡相關性黃斑變性 (AMD)、脈絡膜新生血管 (CNV)、糖尿病視網膜病變 (DR)、視網膜母細胞瘤 (Rb) 和後葡萄膜炎等。

各種眼表、眼前部、眼後部疾病[1]
眼部健康是生命健康的重要組成部分,眼部疾病直接影響視力和生活質量。不同於腫瘤,心血管和糖尿病等重大疾病,眼科用藥市場屬於一個容易被忽視的細分市場。全球眼科領域主要用藥產品集中在幹眼症、青光眼、視網膜疾病、眼部過敏、感染等領域。
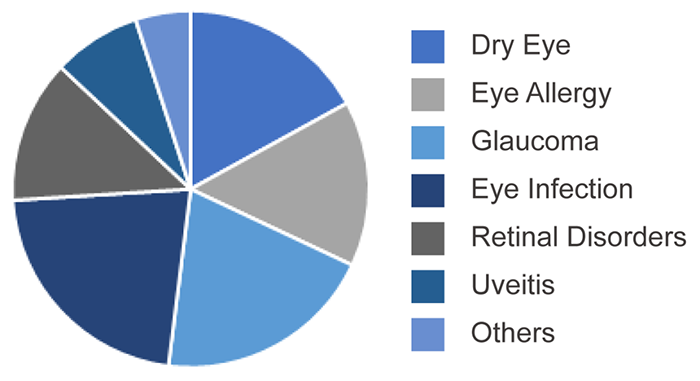
來源:OMR Global
幹眼症
幹眼症 (Dry Eye Syndrome, DES),又稱為角結膜幹燥症,是眼表的一種多因素疾病,特征是淚膜穩態的喪失並伴有眼表症狀。幹眼症的症狀主要為眼部的幹澀感、異物感、灼熱感、眼部常伴有黏稠分泌物。幹眼症的治療包括治療淚液功能不全和分泌異常、消炎藥物、手術、調整飲食、環境因素和補充療法。具體治療方式的選擇以其輕重程度和致病因素為依據。
幹眼症市場情況
幹眼症是全球性問題,亞洲幹眼發病率居全球前列。根據弗若斯特沙利文數據,我國的幹眼症患者人數將近2.35億人,其中18%為中重度的幹眼症患者,預計2030年將增長至2.7億。
美國FDA批準用於治療幹眼症的有:Allergan公司的Restasis、諾華的Xiidra和Kala製藥的Eysuvis、Sun Pharma的Cequa。歐洲上市產品有Santen Pharma的Ikervis。國內幹眼症用藥市場份額領先的前幾個藥物是玻璃酸鈉滴眼劑、重組牛堿性成纖維細胞生長因子滴眼劑和凝膠、及聚乙烯醇滴眼劑等。
幹眼症藥物概述和舉例
幹眼症類型多樣,主要分為水液性淚液不足幹眼症和脂質性淚液不足幹眼症。前者主要是由於幹燥性角、結膜炎導致,而後者主要是脂質阻塞終端導管導致。幹眼症的患病原理及發病機製較為複雜,主要可歸因於炎症、細胞凋亡、神經調節異常及性激素失調,此外病毒感染或角膜塑形鏡不當使用也可能引發幹眼症。目前幹眼症治療多以藥物為主,主要有抗炎治療、人工淚液、角膜修複、促黏液蛋白分泌等。
環孢素: 是一種免疫製劑抗炎用藥,通過抑製鈣調神經磷酸酶起到抑製T細胞活性的作用。目前主要應用濃度有1%和0.05%,1%濃度主要用於抑製角膜移植後的排異反應,0.05%濃度用於幹眼症治療且不引起角膜病變等副作用。
人工淚液: 國內臨床上用於治療幹眼症的藥品中占比最大的就是人工淚液,是目前主流的治療方法,代表性藥物主要包括玻璃酸鈉、羥丙甲纖維素、羥糖甘、聚丙烯酸凝膠、羧甲基纖維素等。其中玻璃酸鈉市占率最高,其原理是利用與人體淚液較為相似的物質緩解幹眼症酸澀疲勞症狀。人工淚液的成分多種多樣,但大部分都隻是起到保養淚膜和暫時性緩解症狀的作用,對於輕度幹眼症患者有一定效果,但無法從根本上治療中重度幹眼症。
視網膜疾病
常見的新生血管性眼病主要有濕性年齡相關性黃斑變性 (wet-AMD)、糖尿病視網膜病變 (DR)、糖尿病黃斑水腫 (DME) 和視網膜靜脈阻塞 (RVO)等。血管內皮生長因子 (VEGF) 與新生血管性視網膜疾病密切相關,也是有效的治療靶點。抗 VEGF 藥物能夠減少新生血管形成,降低血管通透性。VEGFR 是眼科類藥物開發研究得最多的靶點,抑製 VEGFR 功能可有效減少視網膜新生血管化及水腫的發生。在全球眼科藥物市場,由於抗 VEGF 藥物能有效抑製新生血管的形成並促進已有的新生血管消退,已成為眼底血管疾病的主要手段。
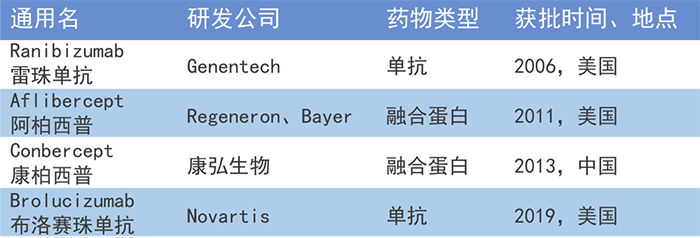
全球已上市的4款抗VEGF眼用生物藥[2]
雷珠單抗 (Ranibizumab): 是一種人源化單克隆抗體片段,可靶向 VEGF-A 的所有同種型。是首個抗 VEGF 眼用生物藥。適應症包括新生血管性 (濕性) 年齡相關黃斑變性(wAMD) 、視網膜靜脈阻塞性黃斑水腫 (MEfRVO) 、糖尿病性黃斑水腫 (DME)、近視性脈絡膜新生血管 (mCNV)等。
阿柏西普 (Aflibercept): 是一種來自人 VEGFR1、VEGFR2、IgG1 的特定結構域的重組融合蛋白。作用靶點為 VEGF-A,VEGF-B,PIGF。適應症有新生血管性 (濕性) 年齡相關黃斑變性 (wAMD),視網膜靜脈阻塞 (RVO),糖尿病性黃斑水腫 (DME) 和糖尿病性視網膜病變 (DR) 等。
康柏西普 (Conbercept): 是由 VEGFR1、VEGFR2 和部分 Fc IgG1 胞外結構域組成的重組人融合蛋白,作用靶點為 VEGF-A,VEGF-B,胎盤生長因子(PIGF) 。是中國首個獲得世界衛生組織國際通用名的生物製品Ⅰ類新藥。適應症包括新生血管性 (濕性)年齡相關黃斑變性(wAMD) 、繼發於病理性近視的脈絡膜新生血管 (pmCNV) 引起的視力損傷、治療糖尿病性黃斑水腫 (DME) 引起的視力損傷。
布洛賽珠單抗 (Brolucizumab): 是一種靶向 VEGFA 的新型抗 VEGF 藥物。是一個單鏈抗體片段。是首個可以間隔3個月給藥的抗 VEGF 藥物。適應症為新生血管性 (濕性) 年齡相關黃斑變性 (wAMD) 。
國外競爭如火如荼,國內多家藥企也在積極開展眼部疾病用藥的臨床試驗。如百奧泰、信達生物、齊魯製藥等。
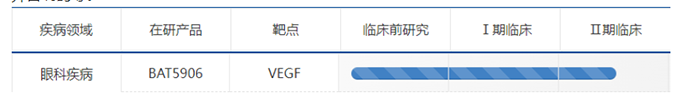
來自百奧泰官網
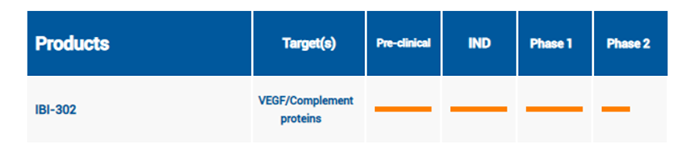
來自信達生物官網
青光眼
青光眼是導致不可逆視力喪失的主要原因。青光眼是一組以視網膜神經節細胞進行性退化為特征的視神經病變。通常到相對晚期才出現症狀,導致診斷經常延遲。神經節細胞的丟失與眼壓水平有關。所以降低眼壓是治療青光眼的有效方法。
青光眼可分為兩大類:開角型青光眼和閉角型青光眼。在美國,80%以上的病例是開角型青光眼;然而,閉角型青光眼導致大量嚴重視力喪失。開角型和閉角型青光眼都可能是原發性疾病。繼發性青光眼可能由外傷、某些藥物 (如皮質類固醇) 、炎症、腫瘤或色素分散或假性剝落等疾病引起。
降壓藥物應以最少的藥物劑量和最小的副作用達到目標眼壓。藥物選擇會受到成本、副作用和給藥方案的影響。一般來說,前列腺素類似物是一線藥物。通過降低流出阻力來降低眼內壓,從而導致通過葡萄膜鞏膜通路的房水流量增加。且幾乎沒有全身性副作用。但是會引起局部不良反應,如結膜充血、睫毛延長和變黑、眼眶脂肪減少、誘導虹膜變黑和眼周皮膚色素沉著等。另外,青光眼藥物長期使用會產生耐藥性,且不同病人對不同機製藥物的敏感性和副作用不一樣,因此需要新機製藥物聯合使用。
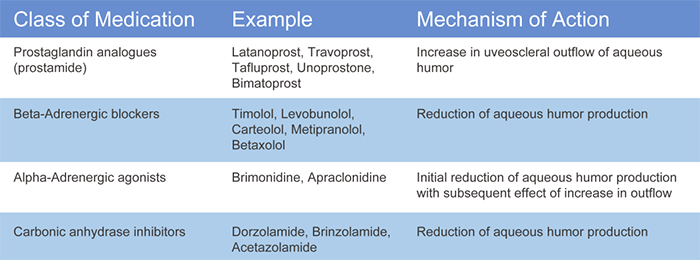
用於降低眼壓的藥物[3]
抗感染、抗炎
可用抗生素進行局部治療的眼部感染一般是前部的淺表感染,如結膜炎、角膜炎和瞼緣炎。導致嚴重結膜炎和角膜炎出現的風險因素包括:糖尿病、免疫抑製、及一些潛在的眼科病理 (如幹燥綜合征、角膜營養不良、角膜移植、近期眼科手術、隱形眼鏡佩戴、淚管阻塞) 和局部皮質類固醇治療等。代表性的治療產品有地塞米鬆、左氧氟沙星等。

局部眼科製劑舉例[4]
挑戰與展望
血眼屏障保護眼睛免受異物的傷害,但同時也限製了分子向眼內腔的滲透,導致眼內治療效率低下。由於眼睛特殊的生理屏障和結構,導致眼部疾病的診斷和治療效率低,缺乏特異性。因此親脂/水性質、透膜性、電荷等因素都是貫穿藥物設計始終的考量要點。
抑製 VEGF 雖然具有顯著的治療有效性,但係統性阻斷 VEGF 通路會伴隨副作用的發生。另外,目前治療手段多為眼內注射,患者依從性較差,因此需要從藥物分子結構設計、劑型改良創新。因此,開發創新的眼部疾病診斷和治療方法正受到高度關注。比如括基因治療、幹細胞療法等。相信隨著對機製的不斷深入探索以及相關技術的不斷優化,眼科用藥會迎來更多突破,為更多患者帶來看見的希望!
參考文獻:
[1]. Sherif A Gaballa, et al. Corticosteroids in ophthalmology: drug delivery innovations, pharmacology, clinical applications, and future perspectives. Drug Deliv Transl Res. 2021 Jun;11(3):866-893.
[2]. Stephanie M Kaiser, et al. Current and Future Anti-VEGF Agents for Neovascular Age-Related Macular Degeneration. J Exp Pharmacol. 2021 Sep 29;13:905-912.
[3]. Robert N Weinreb, et al. The pathophysiology and treatment of glaucoma: a review. JAMA. 2014 May 14;311(18):1901-11.
[4]. Victoria Aramă. Topical antibiotic therapy in eye infections - myths and certainties in the era of bacterial resistance to antibiotics. Rom J Ophthalmol. Jul-Sep 2020;64(3):245-260.
[5]. Yuhua Weng, et al. Nanotechnology-based strategies for treatment of ocular disease. Acta Pharm Sin B. 2017 May;7(3):281-291.
[6]. Kuei-Ju Cheng, et al. Ocular Disease Therapeutics: Design and Delivery of Drugs for Diseases of the Eye. J Med Chem. 2020 Oct 8;63(19):10533-10593.
聯係我們:
電話: +86 (21) 5859-1500(總機)





















 相關新聞
相關新聞