
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com





在剛剛閉幕的全國人大代表大會上,不少醫衛界代表、委員紛紛提出了有關眼底疾病的建議和話題。無獨有偶,去年頒布的“十四五”全國眼健康規劃(2021-2025年)中眼底病首次被提上國家戰略,將眼健康作為提高國民健康水平的重點工作內容。
我國眼健康現況確實嚴峻,中國是全球眼病患者最多的國家。隨著我國老齡化趨勢的發展,白內障、青光眼、幹眼症的患病人數呈現上升趨勢,由高血壓、高血糖引發的視網膜病變患者年齡也在逐漸年輕化。近視是最常見的眼部疾病,目前我國近視患者人數已超6億人,近視率高達48.5%,而且青少年近視率甚至過半[1]。

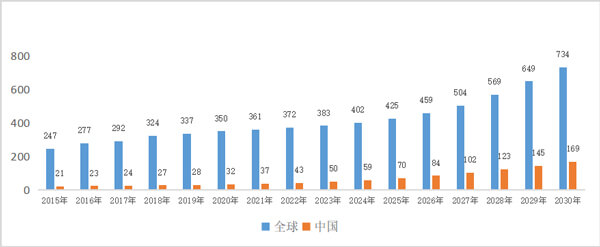
麵對持續走熱的眼科話題,我國的眼科藥物發展迅猛,但依然還無法滿足市場的需求。根據資料顯示,中國眼科藥物市場規模自2015年的21億美元增長至2019年的28億美元,複合年增長率為8%,遠超全球的複合增長率,國內眼科藥物的複合增長率還會持續增長,預計在2030年到達19.1%,國內眼科藥物市場規模達到169億美元[2]。
為了盡快填補市場對眼科藥物的需求,近年來眼科藥物持續獲批,越來越多的藥企加入到眼科藥物的研發和生產中。根據藥融雲數據庫顯示,2014年至今,中國共有234個眼科新藥,其中處於藥物發現階段的藥品共有15個,處於臨床前階段的藥品數量為61個,臨床階段而言,II期臨床的產品最多,達到47個。
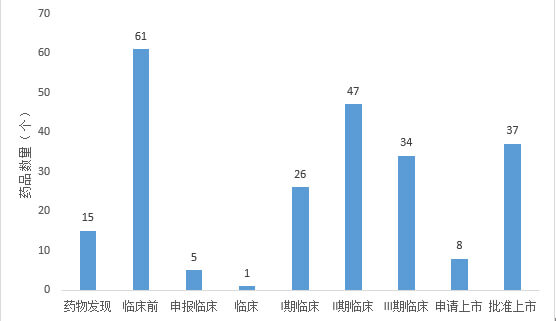
中國眼科新藥研發階段藥物數量(2014年-2022年9月14日)[3]
但由於眼科疾病相關基礎研究進展緩慢,關於藥物的研發,中國主要集中在開發已獲批藥物的改良工藝或劑型上。眼科疾病藥物主要劑型分為:滴眼劑、注射劑、凝膠劑、眼膏劑、片劑藥五大類,其中,滴眼劑長期主導著眼科市場,品類繁多。
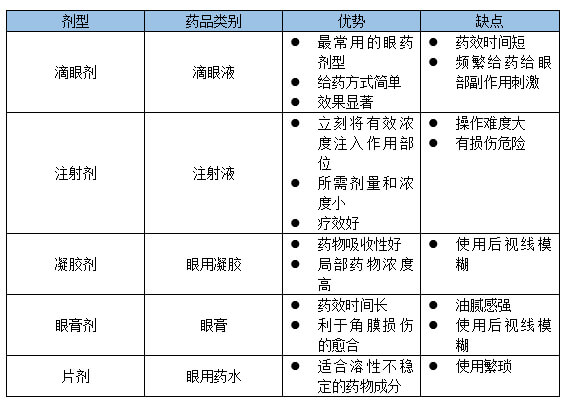
hjc黄金城眼科藥物製劑服務涵蓋滴眼劑、注射劑、凝膠劑、眼膏劑四大類型,完成多款滴眼劑和玻璃體注射新藥的製劑安全性研究並助力獲批臨床。
注射劑眼科藥物由於其給藥方式難度大在研發階段遇到的阻礙比其他劑型大,hjc黄金城的臨床前眼科研究平台可以實現對兔、狗、小型豬及非人靈長類等動物種屬實現獨特的精細給藥,包括:視網膜下腔注射、脈絡膜上腔注射、玻璃體腔注射等,利用多年的豐富實踐經驗和先進設備,解決客戶關於眼科研究的各種複雜問題,專注細節,把控質量,為客戶提供穩定優質的研究服務。
VEGF是眼科類藥物開發研究得最多的靶點,抗VEGF藥物能夠減少新生血管形成,降低血管通透性。在全球眼科藥物市場,由於抗 VEGF 藥物能有效抑製新生血管的形成並促進已有的新生血管消退,其已成為濕性年齡相關性黃斑變性(wet-AMD)、糖尿病視網膜病變(DR)、糖尿病黃斑水腫(DME)和視網膜靜脈阻塞 (RVO)等眼底血管疾病的一線療法。
不管全球還是中國,抗VEGF眼科藥物的研發賽道市場競爭非常激烈。據藥融雲眼科行業白皮書統計,包含批準上市的,全球範圍內有105個,中國有24個。
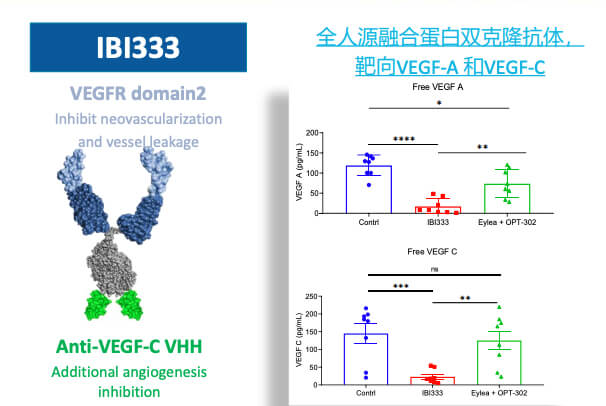
圖片來自:信達生物
2022年9月19日,信達生物自研產品抗VEGF-A/VEGF-C雙特異性抗體IBI333在國內獲批臨床,適應症為新生血管性年齡相關性黃斑變性(nAMD)。這也是全球首款獲批臨床的抗VEGF-A/VEGF-C雙抗。
同時,信達生物管線中還有2款抗VEGFR眼科藥物已進入臨床階段,分別是IBI324(抗VEGF/Ang2雙抗)、IBI302(VEGF/Complement),在國內VEGF靶點賽道上處於領跑位置[4]。
遺傳性視網膜疾病(IRDs)由於大多數導致疾病的基因突變已經被確認,因此基因治療中進展最迅速的適應症領域就是眼科。
其中,以AAV病毒載體為主要應用模式。臨床試驗表明,在眼睛中使用腺相關病毒(AAV)載體遞送基因療法能夠達到治療多種遺傳性眼病的效果且不會引起顯著的免疫反應和全身性副作用。
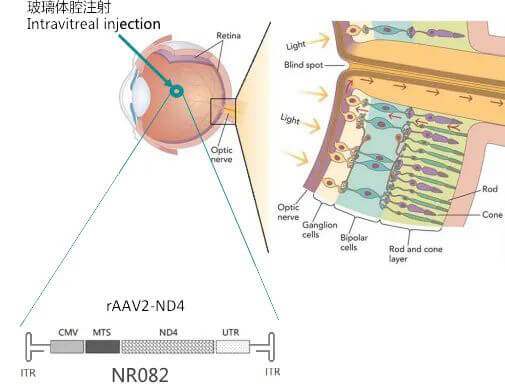
圖片來自:紐福斯生物
2017年12月,眼科用藥市場誕生了第一個基因療法——Spark研發的Luxturna獲批上市。三年後,首個中國自主開發的體內基因治療產品——紐福斯研發的NR082(rAAV2-ND4)獲得美國FDA孤兒藥認證,並在2021年3月在國內獲批開展臨床試驗。
據最新消息,今年2月22日,NR082在中國已完成III期臨床試驗的全部患者入組給藥,期待首個基因治療眼科藥物在中國早日上市[5]!
為了更好地助力行業發展,hjc黄金城將聯合眼科藥物相關企業於2023年04月07日開展眼科藥物線上論壇上半場,展開眼科藥物研發及應用的激烈討論,歡迎各位醫藥同仁參與觀看,還有驚喜好禮相贈!



[1] https://new.qq.com/rain/a/20230308A0A81900
[2] https://www.163.com/dy/article/FG7Q3ILF0519D8QI.html
[3] https://www.pharnexcloud.com/zixun/sd_5239
[4] http://cn.innoventbio.com/#/pline
[5] https://www.neurophth.com/ProjectD-17.html