
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




10月27日,標新生物(Gluetacs Therapeutics)第二個分子膠降解劑管線1類新藥GT929膠囊獲得美國食品藥品監督管理局(FDA)批準進入臨床試驗,用於治療惡性血液腫瘤。
該管線此前已於2023年7月24日獲得國家藥品監督管理局(NMPA)批準開展臨床試驗,預計將在2023年底入組中國I期臨床研究首例病人。
這是標新生物繼GT919後第二個在中美同時獲批臨床試驗的產品管線,是標新生物全球化進程的又一裏程碑。
GT919和GT929用於臨床一期研究的試驗藥物

作為標新生物的戰略合作夥伴,上海hjc黄金城生物醫藥股份有限公司(以下簡稱“hjc黄金城”)為GT929的研發提供了製劑研究、臨床前研究(包括藥效、藥代、安評)以及撰寫中英文申報資料等服務,為GT929快速實現中美雙報雙批提供了技術保障!
分子膠降解劑GT929中美雙報雙批
再次在速度中見證標新實力
標新生物GT929是一款靶向ikzf1/3靶點的分子膠,在彌漫大b細胞淋巴瘤動物模型中顯示了極佳的效果。
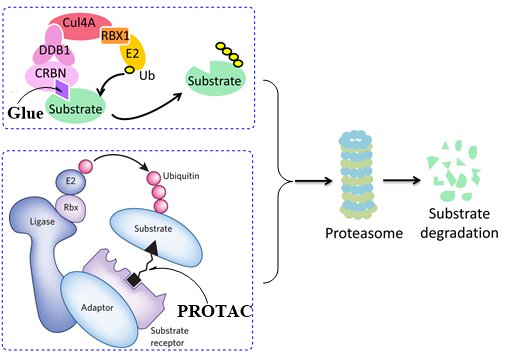
分子膠和PROTAC誘導泛素化的機製
此次GT929新藥實現中美雙報雙批,再次驗證和體現了標新生物GLUETACS™平台快速發現候選藥物和管線推進的能力,也是標新生物全球化進程的又一裏程碑。
再添中美雙報成功案例
hjc黄金城一站式助力創新藥遠航
中美雙報,實現了標新生物GT919、GT929等創新藥的跨國開發,也成為本土藥企走向國際化的重要契機,而擁有中美雙報的GLP資質的實驗室對藥物非臨床研究起著關鍵作用。hjc黄金城作為中國較早提供整套同時符合中國GLP和美國GLP標準的新藥臨床研究申報的CRO公司之一,現擁有2.9萬平方米GLP實驗室。同時,hjc黄金城按照國際標準建立了 Provantis GLP Tox 數據采集係統、EMPOWER 數據采集管理係統、Chromeleon 變色龍色譜數據係統、LIMS 係統強化研究過程的規範性和可溯源性,應用 SEND格式處理數據以確保臨床研究申報滿足 FDA要求。
僅在2023 年上半年,hjc黄金城參與研發完成的新藥及仿製藥項目已有45件通過 NMPA 批準進入臨床試驗,10 件通過美國 FDA 批準進入臨床試驗。(數據來源於hjc黄金城2023年半年報)隨著hjc黄金城參與的按照中美雙報標準要求的項目不斷增加,研究數據與實踐經驗不斷積累,已經成為hjc黄金城核心競爭優勢之一。
hjc黄金城祝賀標新生物GT929臨床試驗申請獲FDA批準,期待GT929臨床試驗順利,早日為全球惡性血液腫瘤帶來新療法。hjc黄金城將持續規範藥物非臨床研究質量管理,對標全球創新藥前沿技術,助力創新藥加速走向世界的征程!
關於標新生物
標新生物(Gluetacs Therapeutics)是一家專注於研發口服蛋白降解小分子藥物的生物醫藥公司,為上海科技大學孵化的首家生物醫藥公司,成立於2020年2月,2021年3月正式運營,由多名在蛋白降解領域深耕多年的科學家領銜創立。公司擁有自主知識產權的分子膠降解劑(GLUE)和雙機製降解劑(GLUETACS)開發平台,並擁有申請和授權不同國家該領域專利近百項,具備獨具特色的差異化技術路線和發展戰略。公司現已自主建立人工智能虛擬篩選平台、體外藥效篩選平台、藥代動力學平台、蛋白質組學平台以及腫瘤動物藥效模型平台,實現了完備的全流程藥物研發體係建設。標新生物自從2021年3月正式運營以來,成功推動兩個候選藥物進入臨床試驗,充分驗證和體現了GLUETACS®平台快速發現候選藥物和管線推進的能力。
 相關新聞
相關新聞