
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




打針或者吃藥就能減肥?一般我們說到減肥,想到的一定是傳統方法“管住嘴,邁開腿”,但通過節食和運動的方法需要長期的過程才能看到效果,對人的毅力也有很大的考驗。以GLP-1為靶點的減肥藥的上市不僅刷新了人們的認知,也在全球減肥市場上掀起軒然大波。
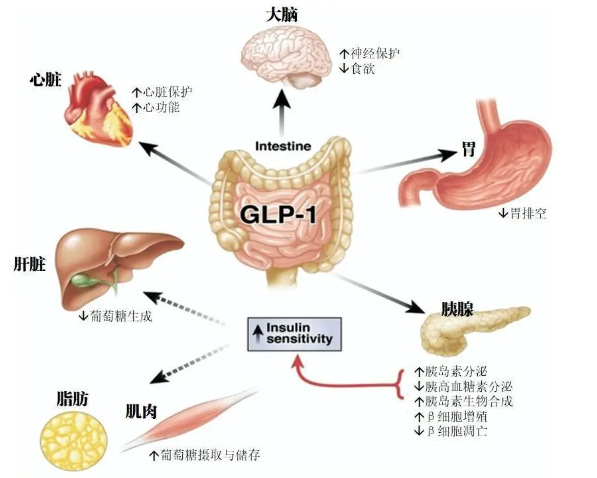
既能降糖又能減肥,另外還有諸多潛在大適應症的探索空間,GLP-1絕對是當今新藥開發的最熱領域之一。從作用原理上來看,GLP-1受體屬於B1類G蛋白偶聯受體(G protein-coupled receptor, GPCR,參與調節體內的血糖水平)。這些藥物模仿腸道中產生的GLP-1激素,向大腦發出已經“吃飽”的信號,抑製中樞係統的食欲和延緩胃排空,讓人不容易感到餓。同時由於這款藥物能鼓動胰髒生產更多的胰島素,降糖效果強,低血糖風險低,對於二型糖尿病患者控製血糖也有裨益。
目前,已經有多款GLP-1類似物獲批上市,據藥智數據統計,全球GLP-1靶點在研管線有184項,涉及企業133家,涵蓋93個適應症。不過大多數都是注射劑,司美格魯肽為諾和諾德研發的產品,在2022年銷售額達109億美元,2023年一季度銷售額為43億美元左右,稱其為“預備藥王”也不為過。同時,口服司美格魯肽作為全球第一款口服多肽類藥物,兼具治療2型糖尿病(type 2 diabetes,T2D)以及減肥的效果,也受到了無數人的追捧。
對於想要減肥的人群來說,口服藥物無疑是一個更方便、更可接受的選擇;而且潛在用戶群體可能會進一步擴大。

近期,諾和諾德在官網公布了司美格魯肽50mg口服片劑的減重IIIa期OASIS 1研究數據。與諾和諾德的司美格魯肽注射劑(Ozempic)相比,小分子口服新藥擁有起效更快和使用便捷的發展潛力[1]。

但從含量和頻率來看,GLP-1藥物的口服生物利用率遠遠低於注射劑。作為多肽類口服藥,有效成分在胃酸環境中容易被破壞失活,因此有包衣製劑方向上的改進研究。想辦法延長藥物的半衰期,將吸引更多的患者和潛在人群的注意力。
GLP-1受體激動劑藥物最常見的不良事件是胃腸道反應,包括腹瀉、惡心和嘔吐。且因為是口服途徑直接接觸胃腸道的原因,口服GLP-1受體激動劑藥物的副作用強於注射劑,並且胃腸道不良事件在劑量升級期間最為突出。對此,糖尿病日報發表的文章建議GLP-1藥物進行更多樣化的劑量研究以找到最佳劑量範圍和給藥頻率,或者讓服藥者根據自身情況製定劑量[3]。
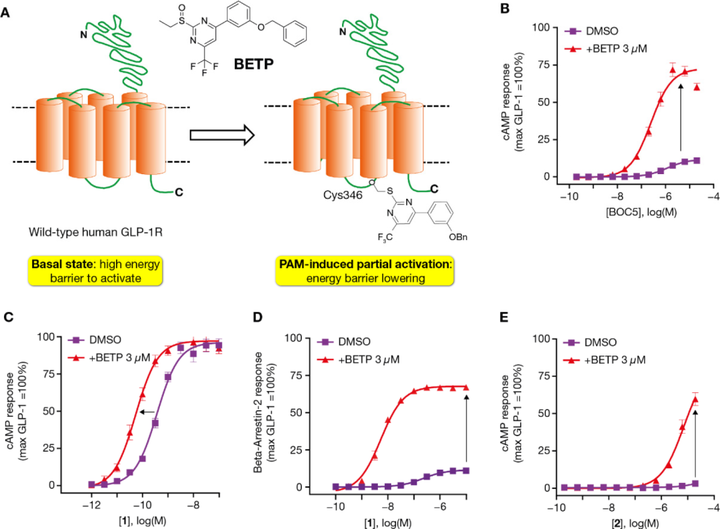
BETP活化受體的設想及驗證[4]
同時,篩選出高活性的前體化合物也是一個研究方向。然而在新藥研發的過程中,性能優良的苗頭化合物的“一票難求”。小分子藥物在發現過程中的苗頭化合物完全依賴於已有的化合物,它們有很多局限性,從中找到理想的苗頭分子需要耗費大量的時間和金錢。這對醫藥研發公司的整個篩選和評價體係要求很高。根據輝瑞在JMC披露的小分子口服GLP-1受體激動劑Danuglipron開發過程,他們通過添加BETP,來降低GLP-1 R向活性構象轉變所需的活化能,高通量篩選280W個分子,篩出了hit分子cmpd 2,>10 μM,然後經過MedChem不懈地優化,得到臨床分子PF-06882961,亦即Danuglipron,1.1 nM[3],其分子量比司美格魯肽及其他多肽降糖藥都要小。
縱觀降糖藥的市場,與諾和諾德在降糖減肥藥市場角逐已久的,是擁有全球首款上市GLP-1受體激動劑艾塞那肽的禮來。不同於諾和諾德司美格魯肽布局的是GLP-1單靶點,禮來率先把目光放在了GLP-1R/GIPR雙重激動劑上,其Mounjaro(Tirzepatide)注射液早在4月就公布了最新3期臨床研究結果,受試者平均減輕15.7%[5]。
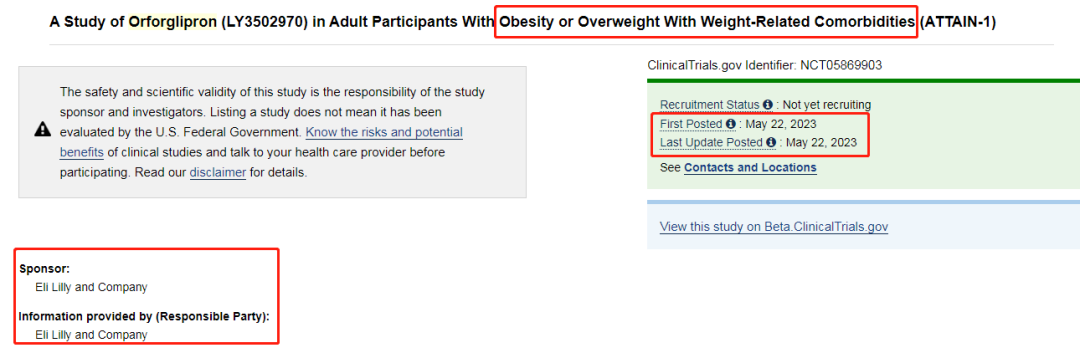
更有意思的是,也許禮來想讓自己“來得正是時候”,在諾和諾德公布研究數據的當日,禮來在clinicaltrials.gov網站上登記了Orforglipron的臨床試驗,啟動了口服GLP-1R激動劑首個減肥III期臨床[6]。並於6月28日在中國獲批Orforglipron的3期臨床,GLP-1紅海市場初見端倪。當今國內藥企同樣不甘示弱,據不完全統計,國內已有海正藥業、華東醫藥、上海仁會生物、質肽生物、麗珠集團等超過10家公司展開布局。據預測,2021年國內GLP-1市場規模達到24.6億元人民幣,預計到2024年GLP-1市場將增長到132.2億元,年均複合增長率67.7%。
7月4日,國內終於迎來首款用於減肥的GLP-1受體激動劑上市,華東醫藥全資子公司杭州中美華東申報的利拉魯肽注射液(商品名:利魯平)肥胖或超重適應證的上市許可申請獲得國家藥品監督管理局(NMPA)批準。GLP-1口服藥物方麵,中美華東的HDM1002片也於5月完成中美雙報獲批。其中hjc黄金城幫助中美華東的HDM1002片完成了製劑工藝和安評的研究試驗。
6月12日專注於使用人工智能驅動新藥研發的德睿智藥宣布,其GLP-1RA小分子口服藥物MDR-001的I期臨床試驗成功完成首例受試者給藥。作為德睿智藥的合作夥伴,hjc黄金城為MDR-001提供了原料藥工藝開發和製劑研發服務。在確保研發質量的基礎上,hjc黄金城通過嚴謹的試驗方案設計、專業化的研發技術、標準化的項目管理、規範化的試驗操作、高效的多方溝通,加速了研發進程,對這一重量級GLP-1R激動劑獲批臨床做出了自己的貢獻。
hjc黄金城依托十九年積累形成的技術優勢和研發平台優勢,圍繞GLP-1新藥研發需求不斷拓展產業鏈上下遊領域,配備有分子克隆室及基於蛋白質晶體學的藥物發現與篩選平台和GMP或非GMP製劑車間,建立了肥胖及糖尿病大/小鼠模型,形成全方位一體化的臨床前CRO服務模式,截至2023年5月底,hjc黄金城已成功助力7個GLP-1藥物獲批臨床,其中3個GLP-1藥物NMPA/FDA同時獲批,1個GLP-1藥物獲得美國FDA、中國NMPA、澳洲TGA三國批準,另外有多個GLP-1項目在研[7],在相關領域積累了豐富的經驗。
參考文獻:
[1]https://www.novonordisk.com/news-and-media/news-and-ir-materials/news-details.html?id=166110
[2] https://www.everydayhealth.com/diabetes/could-this-pill-be-the-next-ozempic/
[3] https://www.diabetesdaily.com/blog/ozempic-users-are-creating-custom-doses-with-or-without-doctors-approval-711475/
[4] A Small-Molecule Oral Agonist of the Human Glucagon-like Peptide-1 Receptor, J Med Chem, 2022
[5] https://www.lilly.com/news/media/media-kits/mounjaro
[6] https://clinicaltrials.gov/ct2/show/NCT05869903?term=Orforglipron&draw=2&rank=2
[7] /news/glp1.shtml
 相關新聞
相關新聞