腫瘤免疫療法是近幾年來癌症治療領域最成功的方法之一,目前主要分為兩個分支:細胞治療免疫和免疫檢查點抑製劑治療(ICB)。免疫檢查點分子是免疫係統中起抑製作用的調節分子,其對於維持自身耐受、防止自身免疫、以及通過控製免疫應答的時間和強度而使組織損傷最小化等至關重要。免疫檢查點分子表達於免疫細胞上,將抑製免疫細胞功能,使機體無法產生有效的抗腫瘤免疫應答,腫瘤形成免疫逃逸。免疫檢查點抑製劑類藥物,可解除這種抑製作用,讓免疫細胞重新激活工作,消滅癌細胞。
然而,令人遺憾的是,免疫治療並不是對每個人有效,隻有一小部分人可以從中獲益(10%-40%,據文章中的數據),雖然研究人員們已經明白這種療法與個體MHC的基因型有著一定的關係,但是根本原因卻尚不明晰。值得關注的是,在年輕和女性癌症患者上, 免疫檢查點抑製療法療效甚微,甚至完全不起作用。
近日,加州大學聖地亞哥分校醫學院的研究人員在Nature Communications 雜誌發表了題為:Strength of immune selection in tumors varies with sex and age的研究論文,發現了一些可以解釋“為什麽年輕的女性患者對某些癌症免疫治療的反應特別低”的證據。

其實,在先前的一些研究中,已經有一些證據累積證明免疫反應存在二型性(dimorphism)。由於基因和激素水平的不同,在注射流感疫苗之後,女性的抗體免疫反應是男性的兩倍並且擁有更多的CD4+ T細胞數。除此之外,女性也更易罹患自身免疫性疾病,表明免疫係統造成的疾病在性別當中也表現出了不平衡。在800多免疫序列測試選擇中,HLA(人類白細胞抗原human leukocyte antigen)的傳播選擇以及CD8+ T細胞的擴增都反映出了性別相關的差異。
不光在性別上,隨著年齡的增加,人體的免疫反應也會隨之減弱。年輕人在大多數情況下具有更強的免疫反應,但這並不意味著癌症免疫療法會對他們更有效。
在此項研究中,研究團隊從美國國立衛生研究院(NIH)的《癌症基因組圖譜》中查閱了近1萬名癌症患者的基因組信息,以及從國際癌症基因組聯盟數據庫和已發表的研究中查閱了其他腫瘤類型的342名患者的基因組信息。
可呈遞的癌症驅動基因更少
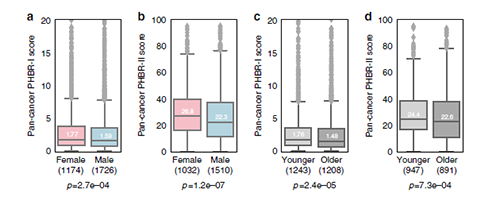
首先,研究人員通過對比MHC-1突變與沒有MHC-1的患者進行對比,發現這些患者中PHBR-1和PHBR-2的分布沒有顯著差別。MHC呈遞的總體相似性表明,診斷時的性別和不同年齡的患者均具有大致相同的癌症驅動基因突變,這意味著由特定等位基因組合產生的MHC呈遞的特異性不是引起ICB應答率差異的機製。
因此,作者認為差異可能是由於免疫選擇強度的差異所致,例如,具有較強免疫編輯能力的腫瘤應保留較少的驅動突變,而這種突變可由患者自己的MHC分子呈現給T細胞。對於每個隊列中的性別和年齡特定組,我們比較了在患者腫瘤中RNA表達的驅動子突變的PHBR-I和PHBR-II的分布。性別和年齡組之間觀察到的癌症驅動基因數量沒有顯著差異,在未觀察到癌症驅動基因突變的病人組中,年輕女性患者的比例過高(費舍爾精確檢驗:I類:OR = 1.12,p < 0.12; II類:OR = 1.28,p < 0.015)。我們注意到,這一組的甲狀腺癌病例過多,這是一種與低突變負擔相關的疾病,通常隻有一個癌症驅動基因突變。因此,我們對2900位獨特的患者進行了針對性別的分析,並對3928位獨特的患者進行了針對年齡的分析。
在整個癌症人群中,女性因其MHC-I和MHC-II分子呈現驅動突變而處於顯著劣勢(PHBR得分較高)。年輕的患者也傾向於通過MHC-I和MHC-II分子表現出更差的驅動基因突變。值得注意的是,組之間PHBR的分布的變化發生在弱結合閾值附近。鑒於有限的體細胞突變會產生突變肽,而且並非所有突變體都是免疫原性的,因此這種微小的變化可能轉化為產生對ICB產生宿主抗腫瘤反應的機會明顯減少。
總而言之,這表明得分差異確實是由遺傳的MHC基因型與觀察到的突變的相互作用造成的。有趣的是,針對女性和年輕患者,映射到這些驅動子突變的RNA外顯子的突變特異性部分明顯更低,進一步支持了免疫選擇中基於性別和年齡的差異強度。
(圖片來源:Nature Communications)
突變信號不能解釋差異選擇
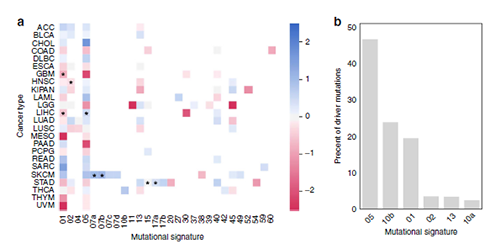
為了排除這種差異是由不同人群接觸的外界突變信號所導致的,作者將特定的突變分配給不同的誘變過程,從而可以探索不同性別和年齡的環境暴露差異。研究人員比較了每種腫瘤類型中突變信號的性別特異性發生率,僅發現少數信號強度較弱但與性別顯著相關的實例。因此這表明環境暴露對免疫選擇對癌症突變基因的性別特異性影響的影響非常低。此外,當排除具有顯著特征差異的腫瘤類型(多形膠質母細胞瘤,GBM和肝肝細胞癌,LIHC)時,研究人員仍然觀察到性別和年齡相關的差異。此外,隻有兩個特征與年齡相關,這兩個特征都與衰老相關聯。我們檢查了C> T和T> C突變,發現在診斷時這些類別中觀察到的癌症驅動局因突變在年齡上分布廣泛。那麽假使老年人的免疫選擇較弱,與其他突變相比,與年齡相關的突變則一定會表現得更好(PHBR得分較低)。相反,在所有可能的MHC-I和MHC-II等位基因中,C> T和T> C突變的表現比其他突變顯著更差(PHBR分數略高)。因此,文章認為 性別和年齡對免疫選擇的影響不太可能是由於環境暴露差異所導致的。
(圖片來源:Nature Communications)
在非TCGA獨立人群中進行驗證
隨後,作者又尋求了從國際癌症基因組協會(ICGC)數據庫中已發表的dbGaP研究和非TCGA樣本匯編的342名患者人群中對我們的發現進行驗證,並過濾以排除TCGA中未顯示的腫瘤類型。盡管相對於發現隊列而言,代表的腫瘤類型較少,但是這些患者在診斷時的性別和年齡方麵各不相同,男性略多於女性,並且平均癌症驅動基因突變數相似。在MHC-I和MHC-II中,年輕女性再次表現出比男性更嚴重的驅動突變(p < 0.001,p < 0.007)。
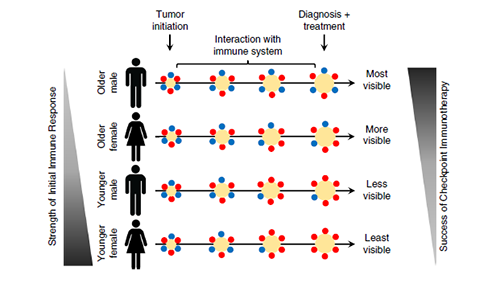
當我們在關注腫瘤免疫療法突飛猛進的新進展,不斷開發新療法的同時,也要明白目前的療法還有很多機理可以進行挖掘,從而使這些新興的生物療法更為我們所用,獲得更好的效果。我們對腫瘤和免疫係統之間的相互作用了解得越多,我們就能更好的針對每個人的情況定製個性化的治療方案。本文通過深入探究性別以及年齡與免疫檢查點抑製劑療效之間的關係,進一步縮小了該療法的適用範圍,在腫瘤個性化的治療上又前進了一步。
參考文獻:
Castro, A., Pyke, R.M., Zhang, X. et al. Strength of immune selection in tumors varies with sex and age. Nat Commun 11, 4128 (2020). https://doi.org/10.1038/s41467-020-17981-0
關於hjc黄金城
hjc黄金城(股票代碼:688202)成立於2004年,總部位於上海,致力於為全球製藥企業、研究機構及科研工作者提供全方位的臨床前新藥研究服務。hjc黄金城的一站式綜合服務以強有力的項目管理和更高效、高性價比的研發服務助力客戶加速新藥研發進程,服務涵蓋醫藥臨床前新藥研究的全過程,包括藥物發現、藥學研究及臨床前研究。hjc黄金城與國內外優質客戶共同成長,為全球超過700家客戶提供新藥研發服務,hjc黄金城將繼續立足全球視野,聚力中國創新,為人類健康貢獻力量!
聯係我們
Email: marketing@yakkaa.com
電話: +86 (21) 5859-1500(總機)
















 相關新聞
相關新聞