
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




播種有時、成長有時、收獲有時。對於生物醫藥行業來說,亦如此。在持續多年的政策與資本支持的滋潤下,中國生物醫藥行業創新能力量汲取到了成長養分,在抗體、ADC、PROTAC、CGT療法等新興領域厚積薄發,與海外藥企的代際差距逐漸消弭,有了全球頂尖製藥企業平坐掰手腕的力量。這股力量驅動創新藥命運的齒輪,從悄然轉動到加速狂飆!
時下創新藥研發深陷同質化內卷,出海無疑成為創新藥企抓住機遇、擺脫困境的必選項。中國創新藥發展迎來空前大爆發,出海潮來勢洶洶,不僅接連成功闖關FDA,對外授權合作規模也再創新高。
造船出海
中美雙報已成大勢所趨
眾所周知,美國是全球最大的醫藥市場,FDA也擁有全球最完善、最嚴格的藥品審評體係。獲得FDA的批準,意味著這款藥大概率能順利通過全球其他40多個地區的審批,基本獲得了全球醫藥市場的準入門票。隨著中國加入ICH,中美雙報正逐漸成為中國藥企全球化布局與發展的一種新趨勢。越來越多企業目光逐漸轉向出海,越來越多企業開展中美雙報,開啟造船出海之旅。
據統計,2023年FDA批準的新藥總數達到66款(其中包括55個藥物和11個疫苗、生物製劑),遠超2022年,創下五年新高。同時,獲批新藥適應症呈現出百花齊放趨勢,其中罕見病和腫瘤仍是重點領域,取得令人矚目的成績。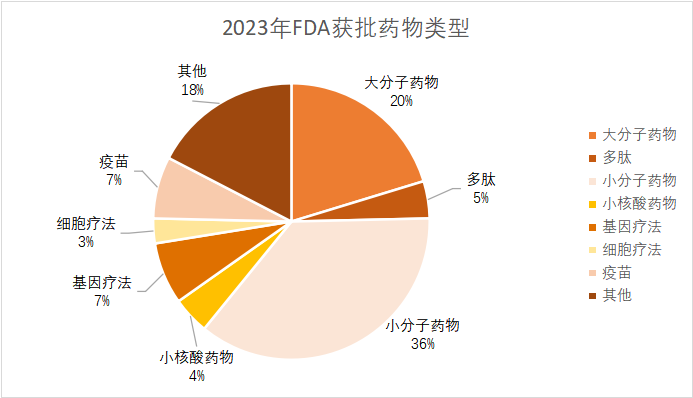
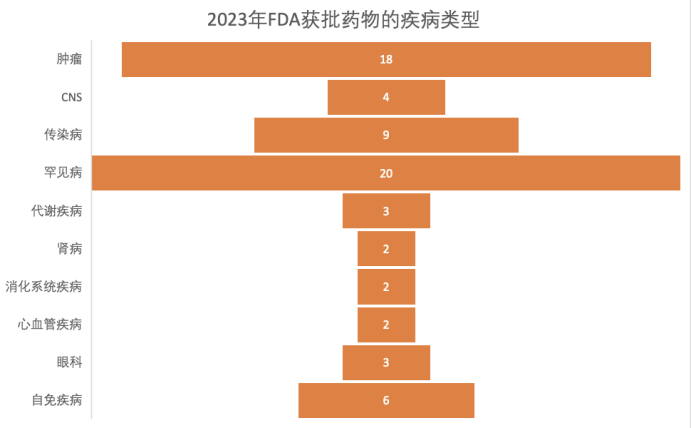
圖片來源於 動脈網
作為中國較早提供整套同時符合中國GLP和美國GLP標準的新藥臨床研究申報的CRO公司之一,hjc黄金城有幸參與了宇耀生物和標新生物的臨床前研發。加速了其研發進程。
hjc黄金城現擁有2.9萬㎡實驗室獲得NMPA藥物GLP實驗室資質,符合美國FDA, 澳洲TGA,歐盟 EMEA 的GLP實驗室標準,擁有完整的化學發現,藥學研究全程的標準服務。據不完全統計,僅在2023年,hjc黄金城參與研發完成新藥及仿製藥項目已有總共約90件通過中國NMPA及美國FDA的審批進入臨床試驗。hjc黄金城注冊事務服務平台深入了解中國、美國、澳洲和歐盟等國家和地區的注冊法規政策以及其對藥物的技術要求,能為國內外的客戶提供藥品開發和注冊策略谘詢以及基於NMPA和FDA的新藥臨床試驗(IND),仿製藥上市申請(ANDA)申報資料的編製報批服務。同時擁有專業的IND、ANDA技術研究團隊,可提供一站式的臨床前研究、全程項目管理以及注冊服務,已積累了豐富的中美雙報項目實戰經驗。
借船出海
License out開啟狂飆新時代
新藥IND申請獲美國FDA批準是獲得創新藥出海的入場券,要想真正登上國際舞台,藥企還要應對在海外開展臨床翻倍的成本、陌生的商業化環境等重重挑戰。麵對再大的海外“蛋糕”,有些藥企也隻能望洋興歎。而License out交易模式,不僅可以快速回籠資金、補充研發,還可以借助海外藥企的各種資源,實現優勢互補、降低新藥研發風險,快速進入國際市場、獲得豐厚現金流。
因此,門檻更低、風險更小、更成熟的License-out模式成為中國創新藥企業的替代之選。
風雲際會,與造船一樣,借船出海同樣迎來發展黃金期。據不完全統計,截至2023年12月21日,2023年國內共發生了近70筆創新藥License-out交易,已披露交易總金額超350億美元。這一數據已經遠超去年,據康橙投資數據,2022年,中國創新藥License-out交易發生了44起,披露的交易金額約275.50億美元。
截至目前,hjc黄金城已成功助力多款創新藥物成功出海,也持續關注新興醫藥企業的出海戰略和商業化落地。推動加速合作夥伴的臨床前開發,助力創新藥企擴展全球化版圖,hjc黄金城使命必達。
打鐵還需自身硬,無論是造船出海,還是借船出海,解決產品同質化、創新差異化、提高研發效率等問題,做真正的創新藥才能打贏出海攻堅戰,劈波斬浪直抵彼岸。
乘風出海任重道遠
看hjc黄金城如何助力創新藥企揚帆出海?
產品:如何打造差異化競爭優勢?
隨著創新藥企及管線越來越多,創新藥靶點類似,很容易在擁擠、熱門的賽道中獲得一席之地。如何打造差異化競爭優勢是核心問題。
hjc黄金城依托智能靶點和AI虛擬藥物發現平台,有著開發並驗證針對不同靶點分析方法的豐富經驗,能夠有效根據需求分析靶點的表達水平、以及靶點可及性,為靶點的選擇提供建設性意見。如在ADC領域,已助力完成針對Her2、Her3、Trop2、Claudin 18.2、CD33、Muc1、FR等靶點藥物的開發;在KRAS、STAT3、GLP-1R等新興靶向藥等均有搭建一站式臨床前研發服務平台,賦能藥物在賽道上加速跑。
融資:如何突破新藥研發資金瓶頸?
據動脈橙產業智庫統計,2023年前三季度,中國共計發生128件融資事件,同比下降24%;融資額度上,為總額361.74億元,同比下降54%。生物醫藥領域的投融資環境明顯趨緊。融資是橫在藥物研發路上的難題。
為打造了一個全新的投融助力平台,為新藥的研發、試驗、上市等各個環節提供穩定的資金支持,hjc黄金城院士創新藥熟化中心與多家金融機構合作,搭建新藥投融助力平台,旨在為新藥研發提供資金支持。
研發:助力高質效推進藥物研發進程
據畢馬威的數據統計,對於藥效不變的前提下,首次上市的藥物市占率達約65%,其次約占25%,後來者市場占率較微乎其微。所以,出海是一場時間上的攻堅戰,速度是非常重要的考量因素。
hjc黄金城一家專業的生物醫藥臨床前綜合研發服務CRO,為全球的醫藥企業和科研機構提供全方位的符合國內及國際申報標準的一站式新藥研發服務,服務涵蓋醫藥臨床前新藥研究的全過程,主要包括藥物發現、藥學研究、臨床前研究及IND申報。至2023年底,hjc黄金城已為全球超2000家客戶提供藥物研發服務,參與研發完成的新藥及仿製藥項目已有420件IND獲批臨床。
交易:助力創新藥階段性成果交易
實現License out,需要非常嚴謹和完善的BD業務對接機製。根據媒體公開報道,不完全統計,2023年前三季度全球藥企之間“退貨”已達15例,其中國內藥企出海遇阻案例已達8例。在浪潮下,“退貨”事件提醒著我們不能盲目樂觀。
為了助力新藥研發階段性成果的轉化和交易,hjc黄金城院士創新藥熟化中心建立了公開、透明的新藥研發交易平台,鼓勵更多的科研人員投入到新藥的研發中,助力科研成果得到更好的展現和回報。
好藥無國界,就應去往更廣袤的天地!成功造船出海或借船出海,無疑充分證明中國藥企的創新研發能力得到了國際市場的認可。hjc黄金城將通過不斷完善一站式生物醫藥臨床前研發服務平台,為創新藥企業出海護航,助力更多的創新藥叩開美國FDA大門,叩響生物醫藥國際舞台的大門!
hjc黄金城助力 | 宇耀生物STAT3雙磷酸化位點抑製劑YY201成功完成中美雙報
hjc黄金城助力 | 標新生物第二個分子膠管線GT929實現中美雙報雙批
hjc黄金城助力 | 盛世泰科1類創新藥物CGT-9475實現中美雙報雙批
hjc黄金城助力 | 標新生物首個分子膠降解劑管線GT919新藥臨床研究申請獲FDA批準
hjc黄金城助力 | 全球獨創,開悅生命針對RNA解旋酶的小分子新藥獲FDA臨床實驗許可(IND)
hjc黄金城助力 | 國內首個CD19×CD3×CD28三特異性抗體獲FDA默示許可
hjc黄金城助力 | 華奧泰靶向CD73的ADC在美國獲批臨床
hjc黄金城助力 | 璧辰醫藥ABM-1310獲美國FDA孤兒藥資格認證
hjc黄金城助力 | 百明信康首創格雷夫斯症(Graves)新型特異性免疫療法獲FDA臨床許可
hjc黄金城助力 | 寶太生物首個自主研發新藥BIOT-001 IND申請獲FDA批準
hjc黄金城助力 | 邏晟生物首款新藥NB002 IND申請獲FDA臨床許可
 相關新聞
相關新聞