
Emai:marketing@yakkaa.com
業務谘詢專線:400-780-8018
Tel: +1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email: marketing@medicilon.com
地址:上海市浦東新區川大路585號
郵編:201299
電話:+86 (21) 5859-1500(總機)
傳真:+86 (21) 5859-6369







© 2023 上海hjc黄金城生物醫藥股份有限公司 保留所有權利 滬ICP備10216606號-3
滬公網安備 31011502018888號 | 網站地圖


業務谘詢
中國:
Email: marketing@yakkaa.com
業務谘詢專線:400-780-8018
(僅限服務谘詢,其他事宜請撥打川沙總部電話)
川沙總部電話: +86 (21) 5859-1500
海外:
+1(626)986-9880(U.S. - West Coast)
0044 7790 816 954 (Europe)
Email:marketing@medicilon.com




hjc黄金城“仿製藥質量一致性評價”服務介紹![]()
“仿製藥質量一致性評價”主要針對2007年新版《藥品注冊管理辦法》頒布實施之前批準的口服仿製藥,主要包括片劑、膠囊劑和顆粒劑等,進行質量再評價。評價要求考察國內企業生產的產品與原研產品在溶出度和有關物質等關鍵質量指標上是否一致。如果質量不一致,則要求企業對產品進行處方工藝改進。
考慮到國內仿製藥質量大多數達不到原研產品的水平,因此“質量一致性評價”的具體業務一般包括兩個部分:
1.對企業產品的溶出度和有關物質與參比製劑進行對比,根據研究數據判斷兩者質量是否一致。
2.如果質量不一致,則需要按照仿製藥研發的要求,對該產品的處方工藝進行重新開發,將開發好的新處方工藝移交給企業並且支持企業進行申報。
仿製藥:是指與原研藥在安全性、有效性、劑量、質量作用與適應症相同的一種仿製品。
仿製藥與創新藥的一致性主要研究內容:
1、生物等效性——體內bloodstream;相同的時間,相同的物質,相同的量
2、臨床一致性
3、質量體係=產品一致性
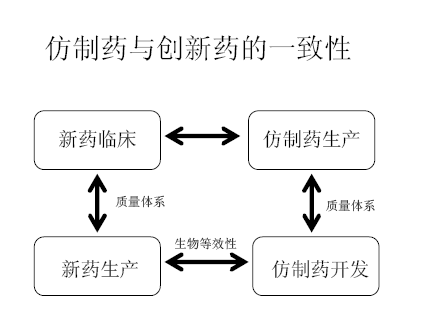
仿製藥和創新藥的一致性
仿製藥質量一致性評價
主要步驟:①體外溶出實驗——藥品檢測機構
②生物等效性——生產企業
質量一致性評價的含義
涵義——狹義:符合相同的質量標準
涵義——廣義:相同的活性成份、適應症、劑型、規格、給藥途徑;符合相同的質量標準、生物等效
注射劑——安全性:有關物質、熱源、細菌內毒素、無菌、異常毒等
口服固體製劑——安全性:有關物質
——有效性:生物等效性
受試製劑與參比製劑溶出或釋放曲線一致時,生物等效的可能性大大增加——關鍵
藥物溶出度試驗是考察、評價製劑內在質量的重要指標。是考察在生產工藝、製劑配方的重要手段。並作為藥物體外-體內相關(invitro-in vivo correlation,IVIVC)、生物等效性(Bioequivalance)與生物有效性(Bioavailability)的評價手段。
※固體製劑口服給藥後,藥物的吸收取決於:藥物釋放,胃腸道的生物膜通透性
※溶出度意義:
(1)、評價製劑批間質量的一致性(2)、指導新製劑的開發
(3)、產品發生某些變更後,如處方、生產工藝、生產場所變更和生產工藝放大後,確保藥品質量和療效的一致性
了解更多 仿製藥質量一致性評價
聯係我們:
郵箱:marketing@yakkaa.com
電話:021-58591500
網址:www.yakkaa.com
 相關新聞
相關新聞